РЕВМАТИЗМ. Острая ревматическая лихорадка, болезнь Сокольского-Буйо.
Опубликовано 20.03.2013 | Автор: oberarzt
Ирина Александровна Зборовская – д.м.н. профессор, профессор кафедры госпитальной терапии с курсом клинической ревматологии факультета усовершенствования врачей Волгоградского государственного медицинского университета, директор Федерального Бюджетного Государственного Учреждения «Научно-исследовательский институт клинической и экспериментальной ревматологии» РАМН, руководитель регионального Центра по проблемам остеопороза, член президиума Ассоциации ревматологов России, член редакционных советов журналов «Научно – практическая ревматология» и «Современная ревматология»
ОРЛ в конце 20 века классифицируется как системное заболевание соединительной ткани с преимущественной локализацией процесса в сердечно-сосудистой системе, развивающееся в связи с острой инфекцией B-гемолитическим стрептококком группы А у лиц, предрасположенных к заболеванию, главным образом у детей и подростков.
Эпидемиология
I. В экономически развитых странах заболеваемость ревматизмом ничтожно мала. В развивающихся странах и в России ревматизм – актуальная проблема практического здравоохранения.
В России в течение последнего десятилетия отмечена разнонаправленная динамика эпидемиологических показателей ОРЛ. Так, в 1992-1994 гг. был выявлен рост первичной заболеваемости по всем формам ревматической болезни сердца с 0,15 до 0,19 на 1000 населения. Увеличение этого показателя было обусловлено учащением случаев ОРЛ, т.е. активной фазы ревматизма с 0,05 до 0,08 на 1000 населения. Изучение этого факта в возрастном аспекте показало, что первичная заболеваемость ОРЛ в целом повысилась за счет роста впервые установленных диагнозов ОРЛ среди детей Северо-Кавказкого региона России, где первичная детская заболеваемость в указанный период составила 0,92 на 1000 детей и была в 6 раз выше, чем в среднем по России (0,16 на 1000 детей). Эти данные подтверждают влияние социально-экономических условий на демографические показатели (упомянутый регион России являлся “горячей точкой”, где происходили военные действия). В последние годы указанные негативные тенденции не повторились.
В настоящее время в России первичная заболеваемость ОРЛ составляет 0,03, а частота впервые выявленных ревматических пороков сердца (РПС) — 0,065 на 1000 населения. Рас¬пространенность ОРЛ и РПС среди детей и подростков составляет 0,5 и 1,3 на 1000 соответственно, среди взрослого населения — 3 на 1000.
В клиническую практику внедрена стройная система диспансеризации и 3-х этапное лечение больных ревматизмом. Все эти мероприятия привели к снижению за¬болеваемости ревматизмом более чем в 3 раза.
Наступила некоторая успокоенность достигнутыми успехами, внимание ревматологов переключилось на другие не менее важные проблемы ревматологии: болезни суставов, системные заболевания соединительной ткани, и в последние 10-15 лет ревматизм как бы выпал из современных ревматологических проблем – “rheumatology sine rheumatism.
Но, как это нередко бывает, подобное благодушие по отношению к ревматизму, занимающему одно из ведущих мест в структуре заболеваемости, причин инвалидности и смертности, особенно в возрасте до 40-50 лет, приводит к негативным последствиям, что и проявилось в 80-х годах неоднократными вспышками острой ревматической ли¬хорадки (ОРЛ) в США, Японии и некоторых европейских странах, отмечающихся дос¬таточно высоким социальным уровнем. Причем, в большинстве случаев диагностика ОРЛ была запоздалой, так как врачи, особенно молодое поколе¬ние, не были готовы распознать это “редкое заболевание” и применить адекватную те¬рапию.
Необходимо отметить также, что за последние годы клинические проявления ОРЛ претерпели существенные метаморфозы с преобладанием в 44-60% случаев маломанифестных форм, когда кардит, артрит или хорея являются изолированными проявлениями первичного ревматизма. Вследствие этого ОРЛ в силу атипичности или “кажущейся редкости”
выпадает из поля зрения молодых врачей, знакомых с ней лишь теоретически и то по полному набору диагностических критериев Киселя-Джонса, что позволило Inhman (1989) высказать мысль о том, что одна из ироний ревматической лихорадки в том, что она исчезает раньше, чем ее поняли. Подобная ситуация приводит к тому, что у 30 % больных, перенесших нераспознанную ОРЛ, формируются пороки сердца.
II. В подавляющем большинстве начало болезни приходится на возраст от 7 до 15 лет. Чаще болеют девочки и женщины (до70 %) и родственники I-ой линии родства.
У большинства больных с пороками сердца, состоящих под наблюдением ревматолога, процесс находится в неактивной фазе. Однако активность начала вновь появляться.
Показатель выхода на инвалидность в связи с ревматическими пороками сердца в начале 90-х годов в среднем по России составил 0,96 на 10000 работающих. По данным специализированных ревматологических ВТЭК Москвы, ревматические пороки сердца являются причиной инвалидности 50% больных.
Учитывая, что по данным эпидемиологических исследований стрептококковая инфекция имеет периодичность со спадами и пиками (всплесками), и что на протяжении последних 100 лет отмечались 3 пика повышения распространенности стрептококковой инфекции, последний из которых наблюдался в 40-х годах и продолжался в течение 10-12 лет с последующим спадом, логично предположить приближение нового всплеска стрептококковой инфекции в начале XXI века. Поэтому углубленное изучение клинических особенностей ревматизма, его этиологии, патогенеза, лечения и профилактики в преддверии нового пика стрептококковой инфекции являются актуальными проблемами современной медицины.
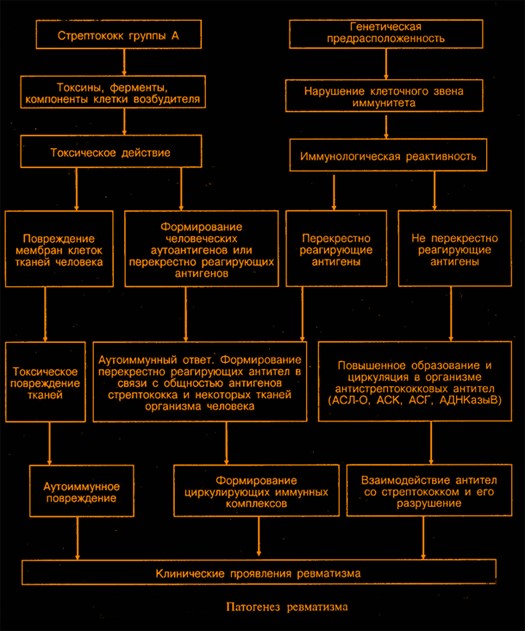
Этиология и патогенез
Причиной ОРЛ является бета-гемолитический стрептококк группы А. После окончания инфекционного воспаления верхних дыхательных путей (фарингит, ангина) стрептококкового генеза развивается осложнение в виде ревматического воспаления, т.е. ОРЛ. В патогенезе ОРЛ важны 3 аспекта: особенности возбудителя заболевания, особенности взаимодействия стрептококка группы А и организма человека и особенности человеческого организма, в котором развивается заболевание.
Бета-гемолитический стрептококк группы А (Streptococcus pyogenes, Streptococcus haemolyticus) представлен в природе 80-ю штаммами. Однако, не все штаммы стрептококка группы А способны вызвать ОРЛ. Известно, что штаммы, вызывающие импетиго, никогда не вызывают ОРЛ. Чаще других с ревматизмом ассоциируются штаммы М1, М3, М5, М6, М14, М18, М19, М24, М27, М29. Предполагают, что эти штаммы стрептококка несут “фактор ревматогенности”, но четких подтверждений этому предположению пока нет. Бета-гемолитический стрептококк группы А имеет большой набор биологически активных веществ, которые секретируются во внешнюю среду или связаны с клеткой, обеспечивая вирулентность стрептококка. Экзогенные токсины ( эритрогенный токсин, гемолизины: стрептолизин-S и стрептолизин – О, гиалуронидаза, протеиназа) обладают пирогенными, цитотоксическими, иммунореактивными свойствами, обусловливающими деструкцию окружающих тканей, выработку антитоксических антител, снижение фагоцитарной активности нейтрофилов. Капсула стрептококка, обладая гидрофильностью, экранирует поверхностные белки стрептококка, что затрудняет распознавание их иммунокомпетентными клетками и эффективность опсонизации возбудителя. В клеточную стенку стрептококка входят различные белки, липотейхоевая кислота, петидогликан, полисахарид. Наиболее поверхностно расположен М-протеин (определяющий штамм стрептококка), являющийся важнейшим фактором вирулентности, которая обеспечивается антифагоцитарной активностью М-протеина. Липотейхоевая кислота вместе с М-протеином входит в состав фимбрий стрептококка, с помощью которых возбудитель прикрепляется к эпителию слизистой оболочки верхних дыхательных путей. Частично липотейхоевая кислота выделяется стрептококком во внешнюю среду в свободном состоянии и оказывает цитотоксическое действие на фибробласты, клетки миокарда и почек. Пептидогликан в комплексе с полисахаридом угнетают миграцию гранулоцитов и микрофагов, оказывают лейкотоксическое и эритротоксическое действие, потенцируют воспалительный процесс в печени, миокарде, синовиальной оболочке.
Не менее важным фактором вирулентности стрептококка являются рецепторы к Fc-фрагменту иммуноглобулина G на его клеточной поверхности, которые способны неспецифически адсорбировать все субклассы иммуноглобулина G человека. Неспецифическая рецепция иммуноглобулина G оказывает антиопсонизирующий эффект. Стрептококк превращается в объект, не распознающийся фагоцитами и иммунокомпетентными клетками. Эффективную опсонизацию возбудителя могут обеспечить лишь антитела, специфически связывающиеся с детерминантами рецептора, или антииммуноглобулины. Поэтому продукция антииммуноглобулинов в инфицированном организме выполняет первоначально защитную роль. с чрезмерным образованием таких антиантител (возможно в результате нарушения супрессорной активности Т- лимфоцитов0 связывают негнойные осложнения стрептококковой инфекции, где стрептококк выполняет пусковую роль в развитии аутоиммунных процессов. Кроме того, доказано, что патогенность или “ревматогенность” стрептококка усиливает его сочетание с вирусом или иерсиниозной инфекцией, переохлаждение, физическое перенапряжение, стресс, хирургическое вмешательство, что приводит к снижению иммунитета и активации латентно персистирующей популяции стрептококков.
Итак, если 30-40 лет назад возникновение ОРЛ ассоциировалось только с перенесенной острой стрептококковой ангиной и невозможностью развития острого ревматизма на фоне хронического тонзиллита, то в настоящее время это положение несколько пересмотрено и расширено с учетом генетических, средовых и других факторов. Понятно, что развитие заболевания связано с острой или хронической носоглоточной инфекцией. Возбудитель – бета-гемолитический стрептококк группы А.
Накапливается все больше данных о роли особых ревматогенных А-стрептококков, в молекулах М-протеина которого наряду с типоспецифическими эпитопами находятся эпитопы, способные перекрестно реагировать с тканями сердца, синовии и мозга. Реализация стрептококковой инфекции происходит с участием феномена молекулярной мимикрии и нарушений клеточно-опосредованного и гуморального иммунитета и обусловлена индивидуальной реактивностью, связанной с семейно-генетической предрасположенностью и носительством В-лимфоцитарного аллоантигена Д8/17.
Центральное место в индукции аутоиммунных реакций отводится антигенам стрептококка, перекрестно реагирующим с антигенами тканей человека. В настоящее время известны сходные антигенные структуры – клеточная стенка стрептококка группы А, мышечная клетка миокарда (кардиальный миозин, сарколемма кардиомиоцитов, фибробласты соединительной ткани сердца) и сосудистая стенка, структурный гликопротеин соединительной ткани клапанов сердца, цитоплазманейронов субталамического и хвостатого ядер головного мозга, эпителий корковой и медуллярной зон тимуса. Представления о наличии “антигенной мимикрии” между антигенными детерминантами компонентов стрептококка и тканями человеческого организма позволяют объяснить все многообразие клинических проявлений ревматизма.
II.Генетическая предрасположенность
Считают, что стрептококковая инфекция, как бы, “запускает” аутоиммунный процесс у генетически предрасположенных людей.
В настоящее время обсуждается мультифакторная (полигенная) природа предрасположенности к ревматизму, связанная с возрастной иммуноэндокринной реактивностью, проявляющейся особой чувствительностью к стрептококковой инфекции, длительностью иммунного ответа на стрептококковые антигены, аутоиммунных реакций, формированию пороков сердца.
Среди лиц, перенесших стрептококковую инфекцию верхних дыхательных путей, ревматизм развивается лишь в 3-4% (в условиях эпидемии) или в 0,3% (при спорадических заболеваниях) случаев. Чаще заболевание возникает в семьях больных ревматизмом (в 3 раза), чем в популяции в целом, что свидетельствует о наличии генетической предрасположенности к ревматизму. В настоящее время выявлен специфический аллоантиген В-лимфоцитов D8/17, являющийся генетическим маркером, определяющим наследственную предрасположенность к развитию негнойного осложнения стрептококковой инфекции в виде ОРЛ, т.е. предопределяющий особую реакцию иммунной системы.
О большей распространенности ревматизма среди родственников больных ревматизмом известно давно, но лишь в последние годы была обоснована генетическая детерминированность этой болезни носительством аллоантигена В-лимфоцитов Д 8/17, который определяется в 96.0-98.0% у больных ревматизмом, в 40.3% – у здоровых кровных родственников, в 66.7% у детей от больных матерей, в 11.8% – у некровных родственников и в 9.5% случаев – у здоровых людей.
Исследования, посвященные изучению ассоциаций ОРЛ с определенными HLA антигенами, выявили большое разнообразие результатов в зависимости от особенностей изучаемых популяций. Имеются данные об ассоциации ОРЛ с HLA антигенами А11, В35, DR2, DR4, DR5, DR7. У больных с поражением клапанов чаще выявляется HLAA3, а при поражении аортального клапана – В15.
III. Сенсибилизация организма
Кроме генетической предрасположенности, для развития ревматического воспаления необходима сенсибилизация организма к стрептококку, т.е. повторное инфицирование возбудителем. Этим объясняется тот факт, что дети раннего возраста (до 3 лет) ревматизмом не болеют.
Таким образом, в развитии острой ревматической лихорадки принимает участие ряд факторов. Бета-гемолитический стрептококк группы А, обладающий ревматогенными, т.е. перекрестно реагирующими антигенами, запускает процессы иммунного воспаления в сенсибилизированном и предрасположенном к нему организме человека.
1. Обусловлена длительной циркуляцией формирующихся иммунных комплексов и их фиксаций в органах и тканях.
2. Многочисленные внутриклеточные и внеклеточные (экзоферменты) антигены стрептококка оказывают непосредственное повреждающее действие на ткани, в том числе на миозин мышечного волокна, воздействует на иммунные регуляции с развитием иммунопатологического процесса.
Опираясь на знания о современных представлениях патогенеза ревматизма Столлерман (1997) дал следующее определение ревматизма: ревматическая лихорадка – постинфекционное осложнение А-стрептококкового фарингита (ангины) у предрасположенных лиц в связи с развитием аутоиммунного ответа на эпитомы стрептококка и перекрестной реактивности со схожими эпитопами тканей человека (в коже, суставах, сердце и мозге).
Итак, развитие ОРЛ определяется:
- прямым токсическим повреждением миокарда “кардиотропными” БГСА- ферментами;
- иммунным ответом на БГСА-антигены, приводящем к синтезу противострептококковых антител, перекрестно реагирующих с антигенами поражаемых тканей человека (“феномен молекулярной мимикрии”).
По- видимому, перекрестно реагирующие антитела, как и многочисленные аутоантитела и ЦИК возбуждают иммунопатологический процесс с отложением иммуноглобулинов и комплемента в тканях сердца и других поражаемых органов, развитием иммунного асептического воспаления и фиброза.
V. Клеточно-опосредованный иммунитет
Однако при ревматическом иммунопатологическом процессе большое значение имеют и нарушения клеточно-опосредственного иммунитета, проявляющиеся в инфильтрации пораженных кардиальных структур лимфоцитами и макрофагами. Макрофаги являются антигенпредставляющими клетками, играющими ключевую роль в местном повреждении и в индукции кооперативного иммунного ответа.
Таким образом, среди механизмов патогенеза ревмокардита большое значение имеют как особая реактивность всех звеньев иммунной системы с продукцией перекрестно-реагирующих антител и ЦИК, их фиксация в тканях, активация макрофагальнолимфоидных клеточных элементов, так и непосредственное повреждение аутологичных антигенов соответствующими антигенами стрептококка с последующим развитием деструкции и фиброза, формированием воспаления кардиосклероза, вальвулосклероза и пороков сердца.
Развитие патологического процесса в соединительной ткани проходит 4 фазы:
1) Мукоидное набухание;
2) Фибриноидное набухание;
3) Гранулематоз (образование ашофф-талалаевских гранулем);
4) Склероз и гиалиноз.
В первой фазе отмечается повышение активности муколитических ферментов, вследствие чего наступает деполимеризация и распад гликозаминогликанов основного вещества соединительной ткани. Происходит накопление гиалуроновой кислоты, обладающей гидрофильностью, за счет чего повышается тканевая и сосудистая проницаемость, ведущая к гидратации и набуханию основной межуточной субстанции. Изменения в этой стадии обратимы, и в случае успешного лечения структура соединительной ткани может полностью восстановиться.
Во второй фазе процессы дезорганизации соединительной ткани усугубляются. В участке ткани, пораженные мукоидным набуханием, проникают белки плазмы, в том числе фибриноген. Образуется аморфная масса – фибриноид, который осаждается и сворачивается в тканях, включая коллагеновые волокна. Одновременно увеличивается проницаемость капилляров, появляются местные очаги некроза. Изменения, происходящие во второй фазе уже не обратимы.
В третьей фазе формируются ашофф-талалаевские гранулемы в результате пролиферации местных соединительно-тканных клеток вокруг очагов фибриноидного некроза, которые являются проявлением специфической клеточной реакции на повреждения соединительной ткани.
Она состоит из крупных, неправильной формы базофильных клеток гистиоцитарного происхождения, иногда многоядерных, гигантских многоядерных клеток миогенного происхождения с эозинофильной цитоплазмой, кардиогистиоцитов (миоциты Аничкова) с характерным расположением хроматина в виде гусеницы, лимфоидных и плазматических клеток, лаброцитов (тучные клетки), единичных лейкоцитов.
Гранулемы носят резорбтивный характер и направлены на рассасывание продуктов распада соединительной ткани. Цикл развития гранулемы составляет 3-4 мес. Гранулемы располагаются в периваскулярной соединительной ткани, интерстиции миокарда (преимущественно левого желудочка), в области сосочковых мышц межпредсердной перегородки, эндокарде и адвентиции сосудов. Ревматическая гранулема – специфический морфологический признак ревмокардита. Однако, в последнее время частота их обнаружения значительно снизилась.
Четвертая фаза завершает процесс дезорганизации соединительной ткани в результате ревматического воспаления и характеризуется эволюцией гранулемы в склероз или исходом фибриноида в гиалиноз (первичный склероз), т. е образованием рубца.
1. Основным морфологическим субстратом поражения сердца при ревмакардите является неспецифическая воспалительная реакция, по существу своему аналогичная таковой в серозных оболочках,суставах. Она складывается из отёка межмышечной соединительной ткани, выпотевания фибрина, инфильтрации клеточными элементами, преимущественно полиморфно-ядерными лейкоцитами и лимфоцитами.
2. При ревматизме наблюдается также поражение мышечных волокон в виде гипертрофии, атрофии, различных видов дистрофии и некробиотических процессов вплоть до полного лизиса с последующей регенерацией функциональных структур миоцитов при стихании ревматического процесса.
3. При сопоставлении данных морфологического исследования со степенями клинической активности ревматического процесса выявлены определённые закономерности.
Так, для максимальной степени активности характерно одновременное поражение нескольких оболочек, сердца и клапанов. Преобладает экссудативный компонент воспаления в виде тромбоэндокардита, экссудативного миокардита, фибринозного перикардита, приобретающего часто диффузный характер. Кроме того, могут обнаруживаться диффузный ревматический эндокардит или вальвулит, описанный В.Т. Талалаевым, возвратно-бородавчатый эндокардит (при непрерывно-рецидивирующем течении). Также отмечают распространенность и выраженность мукоидного и фибриноидного набухания, множественные «цветущие» ашофф-талалаевские гранулёмы.
При умеренной клинической активности преобладает продуктивный тип реакции, часто имеющий очаговый характер (фиброзный, эндокардит, интерстициальный очаговый миокардит), выявляются «стёртые» гранулёмы. По мере уменьшения активности процесса большее значение приобретают дистрофические изменения мышечных волокон, вплоть до появления мелких очагов некробиоза и миолиза. Такие очаги могут расцениваться как метаболический некрозы, с которыми связывают остроразвивающуюся сердечную недостаточность, являющуюся часто причиной смерти таких больных. Обнаружение фиксированных иммуноглобулинов в сарколемме мышечных волокон миокарда и прилежащей саркоплазме, а также в стенке сосудов свидетельствует о роли иммунных реакций в поражении паренхимы сердца.
Морфологическая картина при ревмокардите с минимальной степенью активности процесса по материалам биопсий и патолого-анатомических исследований различная. При изучении биопсий часто обнаруживались гранулёмы и микропризнаки неспецифического экссудативно-пролиферативного компонента. В этих случаях более чем у половины больных после операции выявились признаки активности ревматического процесса.
В случаях ревмокардита с минимальной степенью активности, закончившихся летально, гранулёмы выявлялись редко и более часто отмечались расстройства циркуляции и множественные мелкоочаговые метаболические некрозы.
4. Как правило, почти во всех случаях ревматического поражения сердца (за исключением первичного ревмокардита у детей) обнаруживались склеротические процессы, наиболее выраженные в эндокарде, особенно в клапанном аппарате, где развивался грубый деформирующий склероз.
По частоте поражения на первом месте стоит митральный клапан, затем аортальный и, наконец, трёхстворчатый.
Различают недостаточность митрального клапана, стеноз митрального отверстия и комбинированные пороки с преобладанием того или иного типа порока, в конечном итоге процесс заканчивается стенозом. Митральное отверстие при стенозе может быть в 2-14 раз уже нормы. В миокарде чаще всего развивается склероз соединительно-тканевых прослоек. В склеротический процесс могут вовлекаться волокна проводящей системы.
Участились случаи, когда после ревматической атаки образуется не стеноз или недостаточность митрального клапана, а пролапс митрального клапана.
5. В суставных тканях при ревматическом полиартрите наблюдаются процессы дезорганизации соединительной ткани, экссудатив-ное воспаление, васкулиты с исходом в умеренный фиброз.
В подкожной клетчатке, в области суставов могут возникать располагающиеся группами ревматические узелки диаметром 0,5-2,5см, которые бесследно исчезают в течение 2 нед. – 1 месяца. В сосудах микроциркуляторного русла кожи, особенно в активной фазе болезни, отмечаются воспалительные изменения, периваскулярные скопления тучных клеток лаброцитов, небольшие гистиоцитарные инфильтраты.
6. Серозные оболочки постоянно вовлекаются в процесс при высокой активности ревматизма, давая картину серозного, серозно-фибринозного и фибринозного воспаления.
Помимо неспецифической воспалительной реакции, в эпикарде
происходит организация фибринозных наложений с помощью крупных
гистоцитов, напоминающих клетки ашофф-талалаевской гранулёмы.
7. В интерстиции скелетной мышцы могут наблюдаться как экссудативно-пролиферативные процессы с очагами фибриноидного набухания и реакцией местных соединительных клеток, так и очаговые некрозы мышечных волокон с соответствующей клеточной реакцией из крупных гистиоцитов. Наиболее часто подобные гранулематозные скопления выявляются в мышцах глотки.
8. В лёгких могут наблюдаться изменения, которые расцениваются как ревматическая пневмония: васкулиты и периваскулиты, инфильтрация альвеолярных перегородок лимфоидно-гистиоцитарными элементами, белковые мембраны на внутренней поверхности альвеол, в просвете альвеол-серозно-фибринозный экссудат иногда с геморрагическим оттенком с примесью десквамированных клеток альвеолярного эпителия. Местами встречаются небольшие очажки фибриноидного некроза с крупно-клеточной пролиферацией вокруг (тельца Массона).
9. Поражение почек при ревматизме – проявление системного поражения сосудов. Воспаление и склеротические изменения наблюдаются в сосудах всех калибров, начиная с ветвей почетной артерии и кончая капиллярами клубочков. Наблюдается очаговый, редко диффузный гломерулонефрит.
10. В процесс также вовлекаются все отделы нервной системы. В основе большей части этих изменений лежат васкулиты, которые поражают прежде всего сосуды микроциркуляторного русла.
Атрофические и дистрофические изменения ганглиозных клеток, главным образом подкорковых узлов, имеют место при хорее.
В мягких мозговых оболочках, в строме чувствительных ганглиев, в эндо- и периневрии наблюдаются лимфо-гистиоцитарные инфильтраты .
11. При ревматизме в лимфатических узлах, селезёнке, костном мозге, миндалинах, то есть в “органах иммуногенеза”, отмечается плазмоклеточная реакция.
Период после стрептококковой инфекции является латентным и протекает бессимптомно, либо с признаками затянувшейся реконвалесценции.
В большинстве случаев через 1,5 – 4 недели, после перенесенной стрептококковой носоглоточной инфекции возникает любое из характерных проявлений. Больные часто предъявляют конституциональные жалобы, включающие лихорадку, слабость, быструю утомляемость, потливость, анорексию и уменьшение массы тела.
Острота начальной стадии ОРЛ зависит от возраста больных. В детском возрасте более чем в половине случаев через 2—3 недели после ангины внезапно температура повышается до фебрильной, появляются симметричные мигрирующие боли в крупных суставах (чаще всего коленных) и признаки кардита (перикардиальные боли, одышка, сердцебиение и др.).
Столь же остро, по типу “вспышки”, ОРЛ развивается у школьников среднего возраста, перенесших эпидемическую БГСА – ангину. У остальных детей наблюдается моносиндромное течение с преобладанием признаков артрита или кардита или (редко) хореи.
Для подростков и молодых людей характерно постепенное начало: после стихания клинических проявлений ангины появляются субфебрильная температура, артралгии в крупных суставах или умеренные признаки кардита.
Исключение составляют солдаты-новобранцы, перенесшие эпидемическую БГСА – ангину, у них наблюдается острое развитие заболевания.
Термическая кривая не имеет определенности, отмечаются следующие типы лихорадки:
- одноволновая. выражающаяся одним восходящим периодом, затем стабилизацией и, наконец, спадом, продолжительностью 7-14 дней.
- многоволновая. продолжающаяся в течение недель и месяцев.
- беспрерывная. когда температура постоянно повышена в течении нескольких месяцев, уже не сочетаясь с суставными явлениями.
- гиперпиретическая. представляющая тот тип лихорадки, которая достигает 41-42, но встречается чрезвычайно редко.
Лихорадка подскакивает вверх в зависимости от суставных вспышек и является одним из самых достоверных симптомов. Если лихорадка наступает до появления суставных признаков, ее можно считать продолжением продромального заболевания или выражением латентного кардита. Повышение температуры вне суставных приступов может наводить на подозрение о висцерализации.
Пульс – чаще тахикардия, соответствующая температуре. Тахикардия лишь частично объясняется лихорадкой, чрезмерная и упорная тахикардия может свидетельствовать о кардите.
Брадикардия требует проверки ЭКГ и степени проводимости в a – v узле.
Поты у больного ревматизмом имеют некоторые особенности.
Они обильные, имеют едкий, кислый запах, преобладают ночью и ведут к истощению больного.
Период развернутых клинических проявлений
Затем наступает период клинически развернутой болезни. Центральное место в клинической картине ревматической лихорадки занимает поражение сердца, которое определяет нозологическую специфичность процесса и исход болезни в целом. В патологический процесс возможно вовлечение всех трех оболочек сердца: миокарда, эндокарда, перикарда.
Характеризуется вовлечением в процесс всех оболочек сердца, при этом поражение миокарда – почти обязательный признак болезни. Поскольку на фоне текущего миокардита не всегда легко распознать вальвулит, а тем более пристеночный или хордальный эндокардит, как и нередко стерто-протекающий перикардит, в клинической практике распространен термин “ревмокардит” – обобщающие понятие поражения сердца при ревматизме.
До настоящего времени сведения о частоте поражения миокарда весьма противоречивы. Данные некоторых зарубежных исследователей свидетельствуют о том, что в острой фазе ревмокардит возникает в 3-38% случаев, по другим данным – в 48-73 %. Отечественные ревматологи находят в активной фазе ревматизма кардит в 89-100% случаев. Такую разноречивость в частоте проявления кардита можно объяснить различными методическими подходами и критериями, используемыми клиницистами.
При использовании критериев А.И. Нестерова (1973): увеличение размеров сердца, наличие застойной сердечной недостаточности достаточно сложно диагностировать миокардит при первичном ревматизме, особенно при слабовыраженном кардите.
Подобные критерии кардита применимы лишь при отсутствии пороков сердца, а при возвратном ревмокардите с пороком сердца и развивающихся гемодинамических нарушениях использование этих критериев малооправдано.
Американские кардиологи для диагностики ревмокардита рекомендуют правильное использование диагностических критерием ревматизма Киселя-Джонса: появление новых значительных шумов в сердце, динамика увеличения размеров сердца, перикардит и застойная сердечная недостаточность при исключении других видимых причин. Тем не менее, все эти критерии отражают в большей степени состояние миокарда, а не эндокарда, что в клиническом плане приводит иногда к парадоксальной ситуации, когда у больного на фоне слабовыраженного латентного кардита формируется порок сердца.
Ревмокардит может быть первичным (первая атака) и возвратным (повторные атаки), со сформировавшимся клапанным пороком или без него.
При первичной ревматической лихорадке у детей кардит развивается в 79-83% случаев, у взрослых – в 90-93 % случаев. При повторной ОРЛ у взрослых ревмокардит развивается в 100% случаев.
Ревмокардит характеризуется последовательным вовлечением в патологический процесс миокарда, эндокарда, перикарда. Возможно развитие изолированного диффузного или очагового миокардита, эндомиокардита, панкардита. Клинические проявления ревмокардита определяются преимущественным поражением той или иной оболочки сердца, степенью общей активности ревматического процесса и характером течения заболевания.
Одним из важных критериев ревмокардита, особенно впервые выявленного, является положительная динамика клинических симптомов под влиянием противоревматической терапии.
А.И. Нестеров предложил руководствоваться тремя клиническими градациями ревмокардита: яркий (выраженный), умеренно и слабо выраженный.
Морфологическую основу процесса составляет диффузное, преимущественно экссудативное поражение миокарда, которое у 1/3 больных сопровождается поражением эндокарда, а в 10% – перикарда.
Клинические симптомы ревмокардита.
- Одышка и ортопноз могут отсутствовать при минимально или умеренно выраженном кардите. При достаточной активности процесса часто сочетание с перикардитом.
- Кардиалгия. Характерны длительные колющие, ноющие боли в области сердца, обычно без иррадиации, тяжесть в области сердца.
- Кардиомегалия. В большинстве случаев находят увеличение сердца, не всегда выявляемое физикально. Рекомендуют производить R-графию грудной клетки. При первичном кардите увеличение размеров сердца выявляется в 31% случаев, а при возвратном – 63%.
- Снижение сократительной способности миокарда (выявляется на ЭХО-кардиографии), при первичном – 21%, при возвратном – 31%.
- Характерна обратная динамика увеличения размеров сердца, особенно при первичном ревмокардите.
- Аритмии: ощущение перебоев:
- Синусовая тахикардия (100 и более сокращений в 1 мин.). Число сердечных сокращений регистрируют в покое.
- Фибрилляция предсердий возникает, как правило, при появлении признаков стенозирования митрального клапана.
- Наджелудочковые или желудочковые (редко) экстрасистолы.
- Блокада атриовентрикулярной проводимости с электрокардиографически определяемым удлинением интервала PQ свыше 0,2 с или появлением периодов Венкебаха.
- Снижение звучности первого тона на верхушке сердца, появление 3-го и 4-го тона и шумов, ритм “галопа” – характерные признаки ревмокардита. Нежный “дующий” систолический шум с тенденцией к нарастанию интенсивности и проводящийся в подмышечную область – показание к неотложной активной медикаментозной противовоспалительной терапии Появление новых шумов, динамика ранее существующих.
Низкочастотный мезодиастолический шум:
- лучше всего прослушивается в положении больного лежа на левом боку при задержке дыхания на выдохе;
- при остром ревмокардите с митральной регургитацией часто следует за III тоном или заглушает его.
Базальный протодиастолический шум, характерный для аортальной регургитации, может быть одним из симптомов острого ревмокардита:
- начинается сразу после II тона;
- имеет высокочастотный дующий убывающий характер;
- лучше всего прослушивается вдоль левого края грудины после глубокого выдоха при наклоне больного вперед.
Изолированное поражение аортального клапана без шума митральной регургитации не характерно для острого ревматического кардита, но не исключает его наличия
- Признаки застойной сердечной недостаточности. Редко наблюдают при первичном кардите, намного чаще они сопутствуют возвратному ревмокардиту. Особенно надо обращать внимание на появление застойной сердечной недостаточности у лиц молодого возраста.
По рекомендации АКА, основным критерием ревмокардита является эндокардит, точнее – вальвулит, достоверным признаком которого является возникновение новых шумов при неизменяющихся размерах сердца или изменение существующих шумов.
До настоящего времени нет однозначного ответа по вопросу причин формирования пороков сердца и их прогрессирования. Одни считают, что пороки сердца могут формироваться только в результате активного ревматического процесса и являются исходом ревматического эндокардита, а появление новых пороков сердца или их прогрессирование также могут быть только результатом возвратного ревмокардита (эндокардита). Обострения же ревматического процесса связаны с носоглоточными инфекциями, вызванными стрептококками, к которым организм не имеет типоспецифических защитных М-антител.
Другие считают, что ревматизм является особой формой хронической стрептококковой инфекции с постоянной персистенцией L-форм стрептококков, способных в определенных условиях реверсировать в патогенные формы и предполагают, что, примерно, в 30% случаев атаки ревматизма не связаны с острыми носоглоточными и респираторными болезнями, а обуславливаются неспецифическими факторами: переохлаждением, стрессами, хирургическим вмешательствам и др. которые запускают иммунопатологические процессы и развивается возвратный ревмокардит.
Имеются сторонники гипотезы о прогрессировании пороков сердца и без активации ревматического процесса, считающие, что деформация клапанов происходит за счет гемодинамических нарушений вследствие развития фиброзных отложений на дефектных клапанах, процессов тромбообразования и утолщения створок клапанов.
Они также считают, что в молодом возрасте эволюция пороков происходит за счет рецидивов ревмокардита, а в пожилом – вследствие гемодинамических нарушений и атеросклеротического процесса. Но имеется мнение о том, что тромботические наслоения атеросклеротического генеза на клапанах сердца могут приводить лишь к неполному замыканию клапанов и относительному сужению клапанного отверстия, в то время как в результате ревматического процесса поражается соединительно-тканная основа клапана с вовлечением фиброзного кольца, что приводит к истинному сужению митрального или аортального клапанного отверстия, а “бородавчатые” отложения ревматического генеза на клапанах сердца также приводят к клапанной недостаточности и в то же время служат показателями активного ревматического процесса, его экссудативной фазы.
- приглушение тонов,
- перемещение верхушечного толчка. В результате ревматического вальвулита формируются пороки сердца.
- 78% поражение митрального клапана,
- 7% – поражение аортального клапана,
- 20% – совместное поражение.
Нужно иметь в виду возможность быстрого развития детского первичного стеноза.
Разработаны допплерэхокардиографические диагностические критерии ревматического эндокардита.
Часто сочетается с панкардитом.
Характерно сочетание с плевритом и пневмонией (плевроперикардиальные спайки).
Две формы перикардита:
1-я форма – острый фибринозный (сухой). Для него характерно внезапное начало, сильные боли (иногда задне-грудные, абдоминальные), лихорадка, перикардиальный шум.
2-я форма – экссудативный (серозный) перикардит. Для него характерны: боль “коронарного” типа, диспноэ (соответствующее количеству жидкости), тахипноэ, ортопноэ. С появлением жидкости боль уменьшается, шум трения перикарда также уменьшается или исчезает, глухие тоны. При серозном перикардите иногда возможно раздражение возвратного нерва, в таких случаях больного будет беспокоить кашель. При аскультации – очень глухие тоны сердца. При рентгенологическом исследовании обнаруживается “графинообразная” форма сердца.
Ревматический перикардит имеет благоприятное течение и на фоне противоревматической терапии экссудат быстро рассасывается. Исходом ревматического перикардита могут быть небольшие спайки между листками перикарда, однако, полного их сращения, развития слипчивого перикардита, “панцирного сердца” не возникает, что отличает ревматический перикардит от бактериального (коккового) и туберкулезного.
Типичный реактивный синовит с выпотом жидкости в полость сустава, отечностью и покраснением периартикулярных тканей, иногда с выраженной болью, болезненностью и ограничением активных и пассивных движений.
Характерные признаки ревматического полиартрита :
1. Поражение крупных суставов (коленных, голеностопных, локтевых, плечевых и намного реже – лучезапястных).
2. Симметричность поражения.
3. Мигрирующий, летучий характер артрита (убедиться в этом практически невозможно, так как после назначения лечения в подавляющем большинстве случаев в течение нескольких часов происходит инволюция артрита).
4. Полная обратимость суставного синдрома. Отсутствие изменений на рентгенограммах, восстановление функции суставов.
5. Следует иметь в виду, что ревматические заболевания часто сочетаются, и в клинической картине заболевания часто могут появляться различные “наслоения”. Так, у больного ревматизмом может развиться остеоартрит или ревматоидный артрит со всеми характерными суставными изменениями. Иногда, после повторных ОРЛ симптомы поражения суставов проходят не полностью. В этих случаях развивается фиброз капсул суставов, ульнарная девиация пальцев кисти, формируется артропатия Жаку. Иногда даже с эрозированием суставных поверхностей костей.
6. При ревматизме, чаще при повторных атаках, нередко возникает не артрит, а полиартралгия.
7. В настоящее время установлено, что 25% ревматических артритов – это сейчас моноартрит или поражение мелких суставов кистей и стоп, особенно у юношей. У них же м.б. необычное поражение грудинно-ключичного сочленения.
Ревматический артрит чаще развивается в сочетании с кардитом или хореей. Однако он может протекать изолированно, отличаясь более длительным, чем при типичной ОРЛ, течением, слабым ответом на противовоспалительную терапию. В таких случаях по рекомендациям АКА постстрептококковый артрит, при условии исключения артритов другой этиологии, следует рассматривать как вариант ОРЛ, со всеми вытекающими последствиями в тактике проведения лечения, профилактики и диспансерного наблюдения за больными. В.А. Насонова призывает не переоценивать значение артрита. Если это ОРЛ, то, как правило, симптоматика разнообразна.
Чаще встречается у детей. Нечастое появление ревматического поражения ЦНС, а именно стриарной системы. Может предшествовать первой ревматической атаке, сочетаться с ней или развиваться после нее. Для хореи характерна пентада симптомов: гиперкинезы, мышечная дистония, нарушения статики и координации, сосудистая дистония, нарушения психики. Особенно характерен гиперкинез мышц при их гипотонии.
Клиническая картина складывается из:
- хаотических непроизводных подергиваний конечностей и мимической мускулатуры. Характерно полное исчезновение симптоматики во сне.
- внезапно меняется и психическое состояние ребенка: развивается эгоистичность, эмоциональная неустойчивость или, напротив, пассивность, рассеянность, утомляемость, агрессивность.
- Гиперкинезы проявляются гримасничанием, невнятностью речи, дизартрией, нарушением почерка, невозможностью удержать предметы сервировки стола при еде, общим двигательным беспокойством.
- Вследствие мышечной гипотонии ребенок не может сидеть, ходить, нарушается процесс глотания, физиологические отравления и т.д. (псевдопаралитическая форма хореи).
- Среди отдельных клинических признаков хореи описывают симптомы “дряблых плеч” (при поднимании больного за подмышки голова глубоко погружается в плечи).
- Симптом Черни (втяжение подложечной области при вдохе),
- Симптом “глаз и языка Филатова” (невозможность одновременно закрыть глаза и высунуть язык).
- Симптом “хореической руки” – сгибание в лучезапястном и разгибание в пястно-фаланговых и межфаланговых суставах вытянутой вперед руки.
- Симптом Гордона (задержка обратного сгибания голени при вызывании коленного рефлекса в результате тонического напряжения четырехглавой мышц бедра).
- Хореические гиперкинезы усиливаются при волнениях, реже при физической нагрузке.
- Сухожильные рефлексы при малой хорее несколько повышены, иногда выявляются не резко выраженный клонус стоп.
- При мышечной гипотонии рефлексы отсутствуют.
Диагноз ревматической хореи может быть поставлен невропатологом после исключения других причин поражения нервной системы (системная красная волчанка, хорея Геттингтона и др.)
Кольцевидная (аннулярная) эритема .
Это бледные розовато-красные пятна диаметром до 5-7 см с четкими, не всегда ровными краями. Никогда не зудящие. Встречается у 6-12% больных. Не возвышаются над кожей, бледнеют при надавливании. Характерна локализация на коже груди, живота, спины, конечностей, но не на лице. Спонтанное исчезновение и (редко) рецидивирование. В основе ее лежит васкулит. Не оставляет после себя следов.
Кольцевидная эритема отражает высокую степень сенсибилизации организма к стрептококковой инфекции и поэтому может наблюдаться не только при ревматизме, но и при любых состояниях, обусловленных стрептококком (декомпенсированный тонзиллит, стрептококковый гломерулонефрит и др.).
Узловатая (нодозная) эритема для ревматизма нехарактерна.
Подкожные ревматические узелки
Размером от зерна до горошины с локализацией в периартикулярных тканях могут появиться в период ревматической атаки (их наблюдают у 3-6% больных). В отличие от РА характерно отсутствие центрального некроза. Они не вызывают у больных беспокойства, безболезненны, кожа над ними не изменена. Инволюция узелков происходит в период от нескольких дней до нескольких недель. Иногда они обнаруживаются на затылочной области, области остистых отростков позвонков.
При ОРЛ могут развиваться ревматические серозиты, васкулиты, свидетельствующие как об активности процесса, так и о его системности.
Ревматическая пневмония или легочный васкулит .
Наблюдается преимущественно у детей. Обращает внимание одышка, малая выраженность аускультативной симптоматики при отсутствии притупления перкуторного звука, кашель, лихорадка, отхождение мокроты. Есть тяжелые формы течения. Рентгенологически определяют мелкие множественные очаги уплотнения или двусторонний прикорневой процесс, напоминающий “крылья бабочки”.
При васкулите – кашель, кровохарканье, значительное количество влажных хрипов при аускультации в отсутствие каких-либо перкуторных изменений. Диффузное усиление лёгочного рисунка при рентгенологическом исследовании. Характерна резистентность к антибиотикотерапии, эффективность противовоспалительной терапии. Однако не всегда легко провести дифференциальную диагностику с застойными явлениями в лёгких, особенно при возвратном ревмокардите на фоне порока сердца.
Нередко может развиваться уже в начале болезни, как правило, с небольшим выпотом, регистрируемым рентгенологически.
- Чаще бывает двусторонний.
- Боль в груди, кашель, диспноэ.
- При аускультации: шум трения плевры, лёгкие субкрепитирующие хрипы.
- Для ревматического плеврита характерна большая тенденция к осумкованию (из-за обилия фибрина). При осумковании возникает исчезновение дыхательного шума в нижне-задней области
- Плевральная жидкость – серозно-фибринозная (реакция Ривальта – положительная).
- Обратная эволюция на салицилаты очень хорошая.
Редкий признак болезни, наблюдаемый у детей и связанный с ревматическим перитонитом. Клиническая симптоматика характеризуется внезапным появлением диффузных или локализованных болей в животе, сопровождающихся тошнотой, реже рвотой, задержкой стула или его учащением. Боли носят мигрирующий характер, различные по выраженности, сопровождаются лихорадкой, небольшим напряжением брюшной стенки, болезненностью при пальпации. Перитонеальные симптомы исчезают через несколько дней, обычно рецидивов не бывает.
Поражения почек разнообразны: от преходящего мочевого синдрома (альбуминурия, гематурия) в связи с инфекционным нефритом до диффузного гломерулонефрита.
Маломанифестная симптоматика ревматического гломерулонефрита –главная причина редкой .диагностики в клинике этого системного признака ревматизма.
Нервные проявления (кроме хореи)
В основе лежит васкулит. Возможна острая форма мозгового ревматизма. Характерна головная боль, чувство беспокойства, гипертермия.
Полиневриты, гипоталамический синдром.
Возможен кожный целлюлит с очень болезненной индурацией кожи.
Конъюнктивиты. Эписклериты. Морфологические изменения выступают в виде отека, тургесценции коллагеновых волокон, околососудистой инфильтрации, подконьюктивальной, эписклеральной и склеральной экстравазации эритроцитов в сосудистую оболочку и в реснитчатое тело.
Морфологически выявляют наличие фибриноидного вещества в центре селезеночных фолликул, гипертрофию лимфатических желез. При гистологическом анализе – наличие фибробластов.
Эндокринные сдвиги – это почва для возникновения болезни. Кроме того, эндокринные изменения могут возникать по ходу болезни. Эндокринные сдвиги, как правило, содействуют активации процесса и усугублению сердечной недостаточности. Возможны гипоталамические нарушения. Гипофизарные нарушения, дисфункция коры надпочечников.
Миалгии, интерстициальный ревматический миозит
Для определения активности воспалительного процесса используют следующие лабораторные показатели:
1. Определение числа лейкоцитов – умеренный нейтрофильный лейкоцитоз.
- Ускоренное СОЭ.
- Неспецифические реакции соединительной ткани:
- ↑фибриногена плазмы (выше 0,5 гр. %),
- нарастание дифениламиновой пробы,
- плазматизация костного мозга, нарастание серомукоида,
- появление С-реактивного протеина.
4. При бактериологическом исследовании мазка из зева обнаруживают БГСА. Позитивные результаты микробиологических исследований не позволяют дифференцировать активную инфекцию от стрептококкового носительства.
- Разнообразные коммерческие наборы для быстрого определения БГСА — антигена, хотя и высокоспецифичны, но имеют достаточно низкую степень чувствительности. Серологические исследования, выявляющие повышенные или, что важнее, повышающиеся титры противострептококковых антител, более надежны.
- Нарастание титров противострептококковых антител: антистрептолизин-О (АСЛ-О), антистрептокиназа (АСК), антистрептогиалуронидаза (АСГ).
Во-первых, необходима тщательная оценка ЭКГ-показателей, ФКГ-показателей, ЭХОкардиоргафии.
Установление диагноза ОРЛ – сложная клиническая задача, т.к. нет ни одного строго специфического теста для этого заболевания. С 1940 года используются диагностические критерии ревматизма по Киселю – Джонсу, дополненные Нестеровым. которые постоянно пересматриваются АРА и АКА.
Диагностические критерии Киселя-Джонса-Нестерова
Диагностические критерии подразделяются на основные и дополнительные.
4. Кольцевидная эритема,
5 Подкожные ревматические узелки.
6. Ревматический анамнез – это указание на хронологическую связь болезни с недавно перенесенной носоглоточной (стрептококковой) инфекцией, повторные ангины или ОРЗ, наличие больных ревматизмом в семье, соседей по парте в школе или по рабочему месту на производстве.
7. Доказательство ех juvantibus – эффект лечения антиревматическими препаратами, бесспорное улучшение течения болезни под влиянием 3-5 дневного пробного курса.
Их подразделяют на:
- быстрая утомляемость, раздражительность,
- бледность кожных покровов,
Удлинение интервала PQ на ЭКГ;
Признаки митральной и/или аортальной регургитации при допплер-ЭХО-кг.
Позитивная А-стрептококковая культура, выделенная из зева или положительный тест быстрого определения А-стрептококкокового антигена.
Повышенные или повышающиеся титры противострептококковых антител – АСЛ-О,
Наличие двух больших критериев или одного большого и двух малых в сочетании с данными, документированно подтверждающими предшествующую инфекцию стрептококками группы А, свидетельствует о высокой вероятности ОРЛ; особые случаи: 1) изолированная («чистая») хорея — при исключении других причин 2) поздний кардит — растянутое во времени (>2 мес) развитие клинических и инструментальных симптомов вальвулита — при исключении других причин; 3) повторная ОРЛ на фоне хронической ревматической болезни сердца (или без нее).
Особое значение придают морфологическому подтверждению ревматизма, критерии которого разработаны со времен Ашоффа (1904) и Талалаева (1917). При комиссуротомиях по поводу митрального стеноза у больных ревматизмом этиологический диагноз и степень активности процесса подтверждают биопсией миокарда.
При тонзиллэктомиях ревматический характер тонзиллита иногда обнаруживают при исследовании.
При хорее у умерших устанавливают ревматическое поражение мозга.
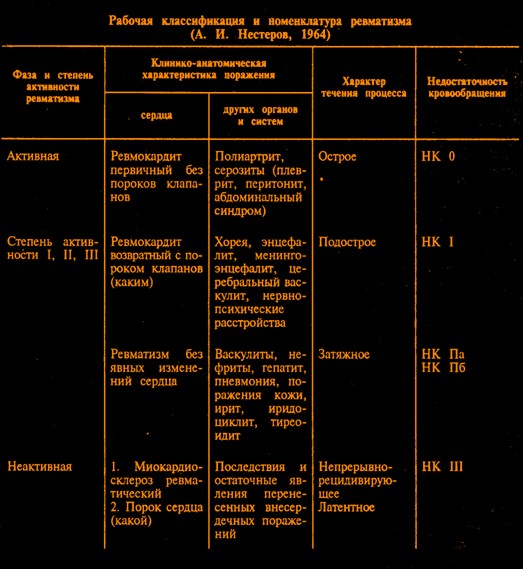
Существовавшая классификация ревматизма предложена А.И. Нестеровым и утверждена на симпозиуме Всесоюзного антиревматического комитета в 1964 г. Классификация предусматривает выделение особенностей клинических проявлений ревматизма, фазы заболевания, степени активности, вариантов течения и осложнений в виде недостаточности кровообращения.
В настоящее время ревматический процесс имеет ряд особенностей. Поэтому в 1996 г. на съезде ревматологов России был предложен новый вариант рабочей классификации ревматизма, в котором современные особенности ревматизма учтены.
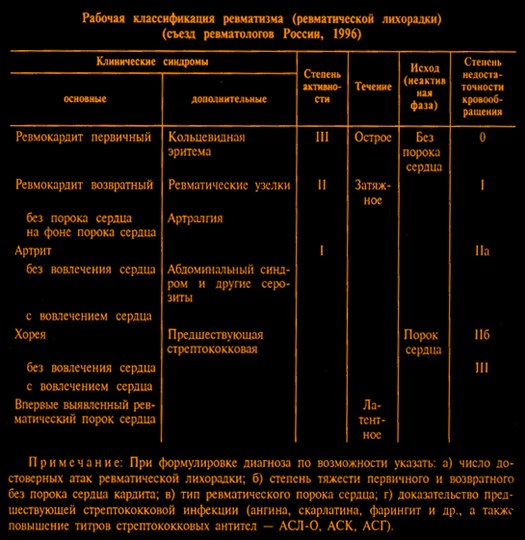
Активная и неактивная фаза. Выделяют 3 степени активности, различающиеся в основном характером воспалительного процесса со стороны различных органов и систем в клинико-лабораторном отображении.
Весьма актуальным является решение вопроса об активности ревматического процесса и неактивной фазе ревматизма.
За рубежом больше сторонников признания ОРЛ как острого заболевания, вызванного стрептококковой инфекцией, и при своевременной диагностике и адекватном лечении происходит полное выздоровление.
У отечественных ревматологов имеются различные взгляды на ревматизм, но большинством признается, и это нашло отражение в отечественной классификации ревматизма, активная фаза болезни, длящаяся в течение 6-8 месяцев при адекватной оптимальной терапии и неактивная фаза ревматизма, характеризующаяся нормализацией всех клинических проявлений и общепринятых клинико-иммунно-биохимических показателей.
В то же время еще с 70-х годов продолжаются дискуссии по поводу правомочности выделения неактивной фазы.
Если ревматизм относить к системным болезням соединительной ткани, на что имеется достаточно много оснований, то ни при одном из известных подобных заболеваний, исходя из существующих классификации, неактивной фазы болезни не имеется, а выделяют лишь периоды клинической ремиссии. Имеются работы отечественных ученых, свидетельствующие о том, что в неактивной фазе ревматизма при операциях по поводу коррекции пороков сердца в биоптатах ушек предсердий гистологически в 70-80% случаев выявляются признаки минимальной активности патологического процесса.
Некоторые исследователи считают, что отсутствие в некоторых случаях специфических гранулем и других признаков активации процесса может быть объяснено наличием у больных очагового ревмокардита, при котором участки с активацией процесса не попадают в биоптат.
Патологоанатомические исследования сердца у больных с прижизненно диагностируемой неактивной фазой ревматизма и умерших вследствие прогрессирующей сердечной недостаточности довольно часто обнаруживали признаки активного ревматического процесса.
Имеются данные о том, что у больных в неактивной фазе ревматизма в 50.0-60.0% случаев в крови определяются повышенные уровни иммуноглобулинов G и М, повышенные титры АСК, изменения активности некоторых энзимов и изоэнзимов.
Многие отечественные ревматологи, вообще, сомневаются в правомочности выделения при ревматизме неактивной фазы болезни и считают, что целесообразнее такую фазу определять как межприступный период. Подобная позиция объясняется тем, что межприступный период, как и неактивная фаза ревматизма, характеризуются отсутствием клинических проявлений, но патологический процесс на клеточном и молекулярном уровне лишь затухает, но не ликвидируется полностью и течет на низком уровне и медленными темпами.
Даже через 6 месяцев перенесенной атаки ревматизма, то есть, в межприступный период, СРБ выявляется в 23,0% случаев, АСЛ-0 – в 55,1%. Не реагировали на в/к введение стрептококкового антигена только 23,0-27,0% больных.
Многие считают, что в межприступный период организм продолжает оставаться сенсибилизированным, и соединительная ткань находится в состоянии гиперергии, что обуславливает ее готовность к рецидивам ревматизма. При тщательном клиническом обследовании у подобных больных можно выявить периодические и нестойкий кардиалгии, артралгии, сердцебиение, лабильность пульса, немотивированную общую слабость, изменение ЭКГ.
Учитывая, что тонкие биохимические и гистологические исследования основного межуточного вещества соединительной ткани свидетельствуют об однотипности его поражения при ревматизме и других системных заболеваниях соединительной ткани, проявляющегося “коллагеновой триадой”: патоморфологические изменения соединительной ткани, плазмоклеточная реакция и гиперглобулинемия, логично допустить, что как при диффузных болезнях соединительной ткани, так и при ревматизме неактивная фаза отсутствует.
Но в то же время имеются данные о том, что при своевременной адекватной терапии, примененной на 1-й ступени ревматического процесса, когда имеется лишь мукоидное набухание, а дезорганизация соединительно-тканных структур поверхностна и обратима (экссудативная фаза), можно не допустить необратимого повреждения и добиться полного выздоровления без дальнейших рецидивов. То есть, возможна и неактивная фаза ревматизма. Но в той же работе авторы придерживаются идеи перманентности течения ревматизма и не признают фатальности его исхода при использовании перманентности терапии (систематичной и поэтапной). Таким образом, мнения по поводу выделения неактивной фазы ревматизма весьма противоречивы, и сторонники ее неприятия придерживаются мнения, что тонкими иммуно-биохимическими и гистологическими исследованиями на молекулярном уровне всегда у больных, перенесших атаку ревматизма, можно выявить признаки активности ревматического процесса, в то время как их оппоненты эти изменения считают следствием гемодинамических нарушений.
Окончательное решение этого вопроса имеет важное значение, так как от него зависит тактика и стратегия лечения больных ревматизмом.

III степень активности.
Как видно из таблицы, клинико-функциональная характеристика и признаки лабораторной III степени активности отражают выраженный экссудативный компонент воспаления.
- Лихорадка,
- Мигрирующий острый или подострый полиартрит,
- Явно выраженный диффузный миокардит, панкардит. Иногда сочетание острого или непрерывно рецидивирующего кардита с симптомами острого или подострого полиартрита, плеврита, перитонита, ревматической пневмонии, гломерулонефрита, подкожными узелками, кольцевидной эритемой, хореи с выраженной активностью.
- Рентгенологически – нарастание увеличения размеров сердца, снижение сократительной функции миокарда, перикардиальные спайки с обратным развитием.
- Четкая ЭКГ-симптоматика. Характерны нарушения ритма и проводимости с динамикой и обратным развитием.
- Лабораторные показатели III степени активности говорят о высокой воспалительной и иммунной активности.
- Как правило, нейтрофильный лейкоцитоз выше 10,0*10 9
- СОЭ – 40 мм/час и выше;
- С – реактивный протеин – 3-4 плюса;
- Нарастание уровня фибриногена – выше 9-10 г/л;
- Серомукоиды > 0,6 ед;
- Повышен уровень гексоз;
- Повышение показателя ДФА-реакции (выше 0,350-0,500);
- Альфа-2 – глобулины > 17 %;
- Гамма – глобулины > 23-25 %;
- Титры АСЛ-О, ACГ, ACK превышают норму в 3-5 раз.
- Характерно повышение проницаемости капилляров 2-3 степени.
- Преобладает умеренно выраженная симптоматика кардита. Может сочетаться о недостаточностью кровообращения I-II степени, медленно поддающийся лечению.
- Подострый или непрерывно-рецидивирующий ревмокардит может сочетаться с подострым полиартритом, моно- и олигоартритом, хореей и т.д.
- Рентгенологически – определяется увеличение размеров сердца, плевроперикардиальные спайки с обратным развитием.
- ЭКГ-симптоматика: Могут быть нарушения ритма, изменение интервала PQ, признаки нарушения коронарного кровообращения с динамикой и обратным развитием.
- Субфебрильная температура. Лабораторные признаки активности. Выражены умеренно.
- Нейтрофильный лейкоцитоз 8*10 9 – 10 * 10 9 .
- СОЭ – 20 – 40 мм/час.
- С – реактивный протеин 1-3 плюса.
- Повышение альфа2-глобулинов до 11—16%.
- Повышение гамма-глобулинов до 21-23%.
- ДФА-проба – 0,250 – 0,300 ед.
- Серомукоид – 0,3 – 0,6 ед.
- То же относится и к показателям противострептококкового иммунитета: повышение титров ACЛ-O, ACK, АСГ в 1,5 раза.
- Повышение проницаемости капилляров II степени.
Для этой степени активности характерна меньшая, чем при III степени активности, тенденция к множественному вовлечению поражённых органов в воспалительный процесс и без выраженного экссудативного компонента воспаления.
При минимальной степени активности клинические симптомы активного ревматического процесса выражены слабо, иногда едва выявляются. Почти полностью отсутствуют признаки экссудативного компонента воспаления в органах и тканях. Характерен преимущественно моносиндромный характер воспалительных поражений.
- Затяжной, минимально выраженный ревмокардит. Может быть недостаточность кровообращения на фоне ранее развитого порока, плохо поддающаяся лечению.
- Может быть затяжной ревмокардит в сочетании с неврологическими изменениями, стойкой артралгией.
- R-ая картина: При первичном ревмокардите нормальные или несколько увеличенные размеры сердца, плевро-перикардиальные спайки с трудным обратным развитием.
- На ЭКГ – может быть нарушение коронарного кровообращения При возвратном ревмокардите – признаки миокардиосклероза, нарушения ритма, с трудом поддающееся обратному развитию.
- Лабораторные показатели нормальны или незначительно изменены
- СОЭ – несколько увеличена, если нет декомпенсации, или нормальная.
- С-реактивный протеин – не выявляется или один плюс.
- Гамма-глобулины слегка увеличены или верхняя граница нормы.
- ДФА-проба – в пределах высокой нормы.
- Серомукоиды – норма (при декомпенсации – понижены).
- Серологические показатели слегка повышены или нормальны
- Повышение проницаемости капилляров I- IIстепени.
Таким образом, возникают большие трудности диагностики I степени активности. В данном случае необходима и важна динамичность исследований. Всё это требует дополнительных диагностических поисков, особенно при минимальной активности.
Используются следующие методы:
- определение нейраминовых кислот
- определение фукозы
Перспективным является использование иммуноферментных методов
- Антитела к ДНК, антитела к сердечной ткани, противотканевые антитела.
- Аутореакции на очищенные белки миокарда.
- Ферментная диагностика: МДГ, ЛДГ, изоферменты КФК (III фракция), изоферменты 3-оксибутиратдегидрагеназы (III фракция), изоферменты тирозинаминотрансферразы и церулоплазмина (I-III фракции).
И эти изменения имеют свои объяснения. На фоне патологического процесса происходит высвобождение медиаторов воспаления из метаболитов с образованием активных перекисных радикалов (ОН-группы, перекись водорода, активный кислород). Они оказывают токсическое, повреждающее действие на клетки. Вследствие образования этих соединений происходит значительная активация процесса перекисного окисления липидов, повышение пероксидации липидов. Активность церрулоплазмина и тирозинаминотрансферазы увеличивается (они связаны с системой интерлейкинов), и они связывают токсические радикалы, переводя их в неактивную форму.
Конечно, важно не просто изучение ферментов, а с учётом их участия в метаболизме и в связи с иммунными нарушениями. Перспективно изучение констелляций ферментов, но в связи с субстратными сдвигами и имеющих отношение к тем или иным иммунным реакциям.
В плане перспективы представляет интерес дальнейшая оценка нормальных и соединительно-тканных антигенов, их участие в патогенезе и использование для диагностики.
Важны дальнейшие генетические поиски.
Большую помощь в диагностике ревматического процесса может оказать и использование новых иммуноферментных методов: метод магнитного резонанса.
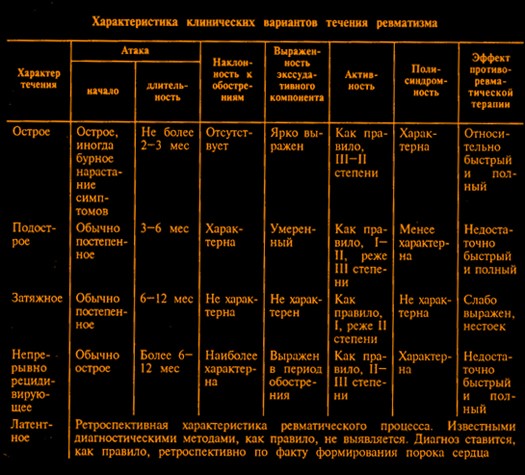
Ранее выделяли 5 основных вариантов течения, распознавание которых базировалось на клинико-временном принципе; остроты начала и длительности течения первичного ревматического процесса или его обострения.
1. При остром течении ревматизма наблюдается острое его начало с лихорадки, полиартрита, ревмокардита, перикардита, с высокой лабораторной активностью и быстрым эффектом противовоспалительной терапии. Цикл клинических проявлений не превышает 2-3 месяца.
2.При подостром течении также может наблюдаться острое внезапное начало, как и при остром» но с менее выраженной лихорадочной реакцией, с менее выраженным полиартритом и с большей стой костью его проявлений и меньшей податливостью к противоревматической терапии.
То же можно отметить и в отношении кардита.
Однако чаще всего наблюдается вообще как бы подострое начало – с субфебрильной температуры, моноолигоартрита, с преобладанием миоэндокардита, с периодическими обострениями и склонностью к течению до 3-6 мес. от начала атаки. В новой рабочей классификации ревматизма – этот вариант течения отсутствует.
3. Затяжное течение – наиболее частый вариант течения возвратного ревматизма – чаще развивается у женщин со сформированным пороком сердца. При этом варианте течения в клинической картине болезни превалирует ревмокардит, сопровождающийся нестойким субфебрилитетом и полиартралгиями. Активность патологического процесса обычно минимальная или умеренная, течение длительное (не менее 6 мес.), монотонное, без четких обострений и ремиссии. Ответ на противоревматическую терапию слабо выражен, не стоек.
4. Непрерывно – рецидивирующее течение.
Оно признается не всеми авторами. Характеризуется возвратом клинических и лабораторных признаков болезни на фоне еще не затухшего ревматического процесса характеризуется волнообразностью.
Каждое обострение чаще всего начинается остро, с вовлечением всех оболочек сердца и (или) с полисерозита, развития васкулитов (легочных, почечных, церебральных), олигоартрита и лихорадки, сопровождающихся лабораторными показателями высокой или умеренной активности.
Противовоспалительная антиревматическая терапия дает неполный эффект, заболевание приобретает как бы затяжное течение, без склонности к ремиссии.
Непрерывно – рецидивирующему варианту течения ревматизма свойственны тромбоэмболические осложнения, обусловленные собственно эмболическим процессами (обычно при мерцательной аритмии), нередкими васкулитами и хроническим диссеминированным внутрисосудистым свертыванием.
Этот вариант течения встречается очень редко. Из рабочей классификации ревматизма, предложенной на съезде ревматологов России в 1996 году, данный вариант течения ревматизма исключен.
5. Латентное течение.
Оно характеризуется отсутствием явных начальных клинических признаков болезни, лабораторная активность не выявляется, но постепенно прогрессирует продуктивное воспаление, исходом которого является порок сердца. Диагноз устанавливается ретроспективно.
Латентный ревматизм может быть первичным и вторичным.
Первично – латентный ревматизм распознается при случайном обнаружении порока сердца (обычно митрального) у лиц, подвергшихся обследованию, например, при эпидемиологических исследованиях.
Вторично – латентный ревматизм может быть установлен при обнаружении признаков прогрессирования ревматического порока сердца у тех больных, у которых нет четких признаков активности, но в процессе наблюдения и лечения отмечается их динамичность, а также при обнаружении признаков морфологической активности в удаленных при операции на сердце ушках предсердий или в биоптатах других отделов сердца.
По функциональному состоянию кровообращения.
Подразумевает подразделение недостаточности кровообращения на I, II (А, Б), III стадии.
Таким образом, рабочая классификация ревматизма позволяет разнопланово оценить фазу ревматизма и конкретизировать активность, как с точки зрения клинико-морфологических проявлений, так и лабораторно – документируемых показателей, оценить характер течения, и тем самым прогноз, и, наконец, функциональное состояние сердца.
И теперь хочу вам представить самую последнюю рабочую классификацию ОРЛ, которая практически узаконена и имеет свои особенности.
Рабочая классификация ОРЛ
- ОРЛ: кардит, полиартрит, АКТ III, Н I.
- Возвратная ревматическая лихорадка: кардит, АКТ I, сочетанный митральный порок сердца, Н II.
- Ревматическая болезнь сердца: комбинированный митрально – аортальный порок сердца, Н II Б.
- Ревматическая болезнь сердца: ревмокардит в анамнезе.
Но от термина постмиокардимический кардиосклероз отказаться!
Во-первых, надо учитывать трудности диагностики РА:
- Кардит, как начальное проявление маломанифестный.
- Не всегда очевиден стрептококковый генез ОРЗ (быстро начинаем лечение антибиотиками).
- Противострептококковые антитела могут быть в низком титре.
- Высеваемость чаще отрицательная.
- Признаки системного воспаления малопоказательны
- Эхо-КГ: более часто диагностируется митральная регургитация, чем при аускультации.
- Помнить об ожидаемом позднем кардите.
В настоящее время существует проблема гипер- и гиподиагностики ревматизма. Диагноз ревматизма нередко необоснованно ставят больным реактивными артритами, ювенильным ревматоидным артритом, геморрагическим васкулитом, саркоидозом, неспецифическими воспалительными и дистрофическими заболеваниями сердечной мышцы, а также при наличии у больных очагов хронической инфекции с вторичными рефлекторными дисциркуляторными и инфекционно-аллергическими проявлениями со стороны сердца и сосудов.
Дифференциальная диагностика ревматизма в ранних стадиях болезни основывается на выявлении полиартрита (моно-олигоартрита) и кардита. Естественно/должны учитываться связь болезни со стрептококковой инфекцией, возраст больного, семейный ревматический анамнез, особенности клинической картины полиартрита. Итак, дифференцировать ревматизм необходимо от клинически сходных заболеваний.
Начинается в молодом возрасте иногда с мигрирующего полиартрита крупных суставов и поэтому, может на первом этапе болезни представлять определенные трудности для дифференцирования с ревматизмом, особенно в тех случаях, когда имеется сопутствующий ревматоидный перикардит или плеврит.
- Для правильного ориентирования при постановке диагноза следует иметь в виду, что при РА в отличие от ревматизма даже при преобладающем воспалении крупных суставов часто бывает более или менее выраженные признаки вовлечения в процесс суставов кистей, стоп и шейного отдела позвоночника.
- Для РА характерна тенденция к хронизации процесса.
- Увеличение лимфатических узлов или селезенки более характерно для РА, а признаки поражения миокарда и особенно эндокарда свидетельствуют о наличии ревматизма.
- У больных ревматизмом применение вольтарена или индометацина приводит к гораздо более быстрому и выраженному улучшению, чем у больных РА.
- Характерна эволюция РА: на первое место выступает хронический суставной синдром.
- Довольно скоро могут развиться при РА атрофия мышц и контрактуры пораженных суставов.
- Анкилозирование не характерно для ревматизма.
- Повышение СОЭ при РА отличается особой стойкостью.
- Титры противострептококковых антител чаще нормальны или снижены.
- Во многих случаях обнаруживается РФ.
- R-ие признаки при РА развиваются позже (остеопороз и т.д.).
Ювенильный ревматоидный артрит.
ЮРА с системными проявлениями нередко бывает весьма сложно отличить от острого ревматизма, поскольку при этих заболеваниях бывают мигрирующий артрит крупных суставов, лихорадка, признаки поражения сердца (в том числе перикардита), боли в животе, повышение титров антистрептолизина.
- Однако нужно иметь в виду, что ревматизму в отличие от ЮРА не свойственны начало болезни в возрасте до 4 лет.
- Боли в шейном отделе позвоночника.
- Для ЮРА особенно важны такие признаки, как “стойкость” артрита от начала его возникновения, вовлечение в процесс других суставов, включая мелкие, нередко симметричный характер поражения.
- Основное отличие ревматического полиартрита от ЮРА мигрирующий характер первого и стойкость второго.
- Типична для ревматического полиартрита довольно быстрое присоединение кардита, высокие титры противострептококковых антител, эффективность противовоспалительной терапии.
- Для подагры характерно в основном моноартикулярное поражение.
- Подагрические узлы. Часто тучность.
- Сравнительно часто встречается при остром лейкозе.
- Причем может возникнуть до появления изменений периферической крови.
- Бактериологическое исследование крови и синовиальной жидкости часто дает отрицательные результаты.
- Дифференциально-диагностическое значение в подобных случаях имеет быстрая и очень высокая эффективность пенициллина без одновременного назначения других средств.
Полиартрит при вирусных инфекциях
При гепатите В правильно ориентироваться в постановке диагноза до развития желтухой позволяют увеличение и чувствительность печени.
Лабораторные показатели нарушения ее функций (в частности, повышение уровня трансаминаз). Обнаружение в крови австралийского антигена.
При краснухе типичны кожная сыпь и увеличение затылочных лимфатических узлов.
Болезнь Лайма. Артрит, кардит, поражения ЦНС (энцефалит) и кожи (хроническая мигрирующая эритема) характерны для болезни Лайма, возбудителем которой является спирохета Borrelia burgdorferi, передаваемая при укусе клеща. Для дифференциальной диагностики необходимы данные анамнеза и серологический анализ на антитела к Borrelia burgdorferi.
Возникают в основном трудности при полиартрическом начале СКВ и при присоединении эндокардита Либмана-Сакса.
- В пользу СКВ говорит: наличие Z, Е-клеток, нуклеарный фактор, накопление антител к нативной ДНК, полиморфизм изменений, нормальный АСЛ-О.
- Малоэффективны при СКВ – салицилаты.
Иногда ОРЛ необходимо дифференцировать от антифосфолипидного синдрома, который может проявляться поражением клапанов сердца и хореей. При дифференциальной диагностике следует учитывать данные анамнеза и результаты определения антифосфолипидных антител.
Фибропластический эндокардит Лефлера .
- быстрое развитие сердечной декомпенсации.
- В формуле крови – лейкоцитоз и эозинофилия.
- Часто путаем с миоартралгией.
- При УП чаще повышается АД и появляются узелки периартериита.
- При УП – 100% поражение почек.
- В пользу дерматомиозита говорит сиреневая окраска кожи.
- Пигментация вокруг глаз.
- Преобладают мышечные боли.
При внезапном возникновении этого синдрома его можно спутать с ревматической атакой. Для него характерно:
- Носительство HLA-B27 антигена
- Неспецифический уретрит после кишечного эпизода.
Постстрептококковый реактивный артрит .
При наличии постстрептококкового реактивного артрита целесообразно кардиологическое обследование и наблюдение за больным в течение как минимум трех лет.
- При возвратном ревмокардите на фоне сформированного порока сердца, особенно аортального, приходится исключать инфекционный эндокардит.
- При этом следует учитывать в ближайшем анамнезе бактериальные инфекции – инфицированные травмы, гнойные инфекции и др.
- При бактериальном эндокардите выражен синдром интоксикации. Больные жалуются на резко выраженную слабость, похудание, познабливание, потливость, боли в костях и мышцах, упорные артралгии или неярко выраженный мигрирующий артрит, периартрит.
- Для бактериального эндокардита характерна длительная ремитирующая, иногда интермиттирующая лихорадка с ознобами, проливными потами, бледностью кожных покровов, «кофе с молоком».
- Появление симптомов деформации ногтей (“часовых стекол”), или ногтевых фаланг (по типу “барабанных палочек”).
- Симптомов Лукина – Либмана.
- Наклонность к тромбоэмболиям.
- Развитие диффузного гломерулонефрита, васкулитов.
- Не связанное с недостаточностью кровообращения увеличение печени – почти такой же обычный симптом при бактериальном эндокардите, как и спленомегалия.
- Важное диагностическое значение придается стойкой прогрессирующей анемизации, значительной гипергаммаглобулинемии, значительно ускоренной СОЭ.
- Повторные обнаружения бактериемии.
- Выявление вегетации на клапанах сердца при ЭХОКГ.
- Для бактериального эндокардита характерен положительный эффект лечения большими дозами антибиотиков.
- В некоторых случаях возвратного, чаще затяжного, ревмокардита возникает необходимость проведения дифференциальной диагностики с тяжелыми прогрессирующими вариантами миокардита Абрамова – Фидлера, при котором наблюдаются бледность кожных покровов, одутловатость лица, цианотично – серый оттенок кожи.
- Интенсивные продолжительные боли в области сердца, нарастающая одышка, слабость.
- Прогрессирующая недостаточность кровообращения, плохо поддающаяся медикаментозной терапии.
- Как правило, обнаруживается тахикардия, гипотония.
- Значительное увеличение размеров сердца, глухость тонов сердца.
- Наряду с мышечным систолическим шумом у некоторых больных можно выслушать мезодиастолический шум, ритм галопа.
- Сравнительно часто выявляются пароксизмы мерцания предсердий, экстрасистолия.
- Реже – пароксизмальная тахикардия, полная и стойкая атрио – вентикулярная блокада.
- Характерным признаком таких форм миокардита являются глубокие электрокардиографические изменения в виде разнообразных нарушений ритма, изменений внутрижелудочковой проводимости, блокады ножек предсердно-желудочкового пучка, тяжелых нарушений а-v проводимости вплоть до полной поперечной блокады.
- Рентгенологически обнаруживают выраженное увеличение всех отделов сердца, снижение амплитуды пульсаций по контуру сердца, зон адинамии при рентгенокимографическом исследовании.
- Характерно несоответствие между тяжестью состояния и полным отсутствием изменений в анализах крови, типичных для острой фазы воспалительного процесса.
Обобщение причин гипердиагностики ревматизма
У лиц молодого возраста, поступивших в стационар с различными заболеваниями сердечно – сосудистой системы, позволяет разделить их на 2 группы:
1 группа. Ошибочная диагностика порока сердца с последующей трактовкой его безусловного признака ревматизма.
Наиболее часто, особенно в поликлинической практике, встречается гипердиагностика недостаточности митрального клапана. Это связано с большой частотой функциональных систолических шумов, не всегда правильно оцениваемых практическими врачами. В детском и юношеском возрасте порок сердца (недостаточность митрального клапана) ошибочно диагностируется при наличии пролапса митрального клапана. Характерная аускультативная картина (наличие в зоне проекции митрального клапана щелчка в середине систолы и следующего за ним позднего систолического шума митральной регургитации), а также данные эхокардиографии (избыточное движение створок митрального клапана в полость левого предсердия во время систолы) позволяют диагностировать пролапс митрального клапана.
2 группа. Нередко наблюдается гипердиагностика ревматизма у лиц молодого ”возраста с наличием у них неревматического миокардита, миокардиодистрофии, нейроциркуляторной дистонии, инфекционного эндокардита и др.
К особенностям синдрома поражения миокарда ревматической природы (синдром первичного ревмокардита) относятся:
- Хронологическая связь заболевания с носоглоточной стрептококковой инфекцией; существование латентного периода длительностью от 10 дней до 2 нед между окончанием предшествовавшей инфекции и первыми клиническими проявлениями ревмокардита.
- преимущественное возникновение заболевания в детском и юношеском возрасте (7-15 лет).
- Острое или подострое начало.
- Частое обнаружение полиартрита или полиартралгий как начальных проявлений болезни.
- Отсутствие кардиальных жалоб и их констатация только при целенаправленном расспросе больного.
- Относительно частое выявление сочетания миокардита, вальвулита, перикардита.
- Высокая подвижность симптомов воспалительного поражения сердца.
- Четкая корреляция выраженности клинических проявлений ревматизма с лабораторными показателями активности ревматического процесса.
Для воспалительного поражения миокарда неревматической этиологии (неревматический миокардит) характерны следующие особенности:
- В отличие от ревматизма развивается в разгар инфекции (ангина, грипп, тиф и др.) или короткий латентный период.
- Быстро достигает максимальной выраженности.
- Прогрессирование и признаки поражения клапанов ему нейсвойственны.
Инфекционно – аллергический миокардит.
- Развивается в отличие от ревматизма чаще после 25-30 лет.
- Латентный период после инфекции короче.
- Частое наличие аллергического синдрома в виде крапивницы, вазомоторного ринита и коньюктивита, лекарственной непереносимости и др.
- Наиболее характерны упорные кардиалгии, сердцебиение, одышка.
- Глухость тонов (особенно I).
- Разнообразная и нередко быстро меняющаяся ЭКГ- картина (в частности, блокады, экстрасистолия, резкие изменения конечной части желудочкового комплекса встречаются чаще по сравнению с ревматизмом).
- Пороки сердца никогда не образуются.
- Особенностью аллергического миокардита является частая диссоциация между отчетливыми сердечными изменениями (явления кардита) и невысокими или чаще нормальными лабораторными показателями воспаления (СОЭ, содержание в крови альфа2 – глобулинов, фибриногена и др.) и отсутствие сопутствующих артритов.
- Медленная динамика клинических и ЭКГ-изменений под влиянием противовоспалительной терапии.
Тонзиллогенная функциональная кардиопатия. (тонзиллокардиальный синдром)
- В отличие от ревматизма в этих случаях никогда не бывает достоверных признаков клапанного порока сердца, отчетливых изменений миокарда.
- Нет выраженных электрокардиографических изменений: нормальные пробы, указывающие на тканевой распад или воспаление, содержание в крови фибриногена, альфа-2 – глобулинов и т.д.
- После консервативного лечения тонзиллита, и особенно после тонзиллэктомии, состояние большинства больных заметно и быстро улучшается.
- У отдельных пациентов, однако, наблюдаются прежние невротические жалобы.
Функциональные заболевания сердечно-сосудистой системы
Дифференциальный диагноз ревматизма (особенно в случаях затяжного возвратного ревмокардита) необходимо проводить с функциональными заболеваниями сердечно – сосудистой системы (функциональной кардиопатией, нейроциркуляторной дистонией, неврозом сердца). Для этой группы заболеваний характерны следующие симптомы:
При неврозах сердца наблюдается эмоциональная окрашенность жалоб, их многообразие.
- Неадекватность жалоб при отсутствии объективной сердечной патологии.
- Наиболее часты жалобы на постоянные боли в области сердца, совершенно нехарактерные для ревматизма.
- Как и при тонзиллогенной функциональной кардиопатии могут отмечаться вегетативные нарушения; могут быть вегетососудистые кризы, протекающие по симпатико-адреналовому или ваго – инсулярному типу, на фоне которых усиливаются кардиальные жалобы – боли в области сердца, ощущение “замирания”, “остановки сердца”, “нехватки воздуха” и др; тахикардия, экстрасистолии (обычно наджелудочковые), снимаемые при назначении обычных седативных средств (валериана, боярышник), либо небольших доз бета-адреноблокаторов или изоптина.
- Отсутствие сформированного порока сердца несмотря на наличие в анамнезе многочисленных “атак ревматизма”.
- Отсутствие эффекта от применения нестероидных противовоспалительных препаратов и улучшение состояния на фоне применения седативных препаратов и транквилизаторов.
Необходимость дифференциального диагноза с тиреотоксикозом возникает редко.
В сомнительных случаях необходимо использовать определение основного обмена, поглощение щитовидной железой радиоактивного I и особенно определение содержания в крови истинных гормонов щитовидной железы ТЗ и Т4.
I. Лечение должно быть трехэтапным, что, к сожалению, не всегда соблюдается.
1 этап. Лечение активной фазы проводят в стационаре.
2 этап. Восстановительное лечение в условиях пригородного санатория или на больничном листе (завершение лечения, начатого в стационаре).
3 этап. Диспансерное наблюдение и профилактическое лечение.
II. Принципиально разделение на активную и неактивную фазу.
III. По-возможности – более ранняя диагностика – при этом лучше эффект терапии.
IV. Раннее начало лечения.
V. Комплексная терапия (этиологическая, патогенетическая, восстановительная, симптоматическая.
Больной находится в стационаре 6-8 недель при первичном кардите, и даже более – при возвратном (в среднем 40-45 дней).
Этот этап включает в себя:
- Общий режим.
- Питание.
- Медикаментозное лечение.
- Лечебная физкультура.
- Иногда – хирургическое лечение.
В первые 7-10 дней больной при лёгком течении должен соблюдать полупостельный режим.
Весь период острых и подострых явлений и при выраженных явлениях кардита – строгий постельный режим.
Длительность строгого режима определяется общими показаниями болезни, степенью поражения сердца и недостаточностью кровообращения.
Критерием расширения двигательного режима являются темпы наступления клинического улучшения, нормализация СОЭ и других лабораторных показателей. При полиартрите и хорее без кардита постельный режим не назначают.
Ко времени выписки больного следует перевести на свободный режим, близкий к санаторному. Кроме того, желательно, нахождение в тёплых (18-20°) и малых палатах.
- Диета должна соответствовать столу № 10.
- Эти больные не нуждаются в специфической диете.
- Необходима достаточно калорийная и легкоусвояемая пища.
- Ограничение жидкости и поваренной соли (на 1/3 или 1/2), особенно при недостаточности кровообращения и назначении гормонов.
- Желательно некоторое ограничение углеводов, особенно в периоде начинающейся клинической ремиссии.
- В связи с дезорганизацией соединительной ткани и белкового метаболизма необходимо: 1-2 г белка на 1 кг веса.
- Жиры можно и нужно.
- Витамин С. Он участвует в строительстве основного вещества соединительной ткани, в фибриллярных элементах, а также в синтез гормонов надпочечников, в окислительно-восстановительных процессах. Необходимо 0,3-0,6 г и выше в сутки, так как возникает дефицит витамина С в течение 1 – 1,5 месяцев, а далее в половинной дозе до 12 недель.
- Витамин B1 – 1,0 мл 6% раствора
- Витамин В6 – 1,0 мл 5% раствора в/м через день в течение одного месяца.
- Соли калия (фрукты, овощи). Они необходимы для работы мышцы сердца, оказывают мочегонный эффект.
Принципы медикаментозной терапии:
- Использование средств и методов десенсибилизирующей и анти воспалительной терапии.
- Восстановление общей реактивности организма.
- Симптоматическая терапия (при недостаточности кровообраще ния и т. д.).
- Борьба с очагами инфекции.
- В последующем – функционально-восстановительная терапия.
- противовоспалительное и десенсибилизирующее действие;
- влияют на повышенную проницаемость капилляров, клеточные мембраны;
- угнетают выработку антител;
- снижают процессы сенсибилизации и аутосенсибилизации.
Показания к применению гормонов :
Несмотря на противоречивое отношение к назначению кортикостероидов, считают, что кортикостероиды показаны:
- при первичном кардите, при II – III степени активности с выраженным экссудативным компонентом воспаления, когда особенно высок риск формирования клапанного порока сердца;
- у больных возвратным ревмокардитом при подозрении на прогрессирование вальвулита;
- при декомпенсации – гормоны лучше там, где она связана с кардитом, с активностью, иначе они содействуют дистрофии.
Глюкокортикостероиды не применяют при минимальной степени активности ревматического воспаления, и слабо выраженном кардите, если он не первичный. Чаще других препаратов используют преднизолон, а при возвратном ревмокардите на фоне порока сердца – триамсинолон. Преднизолон назначают в начальной дозе 0,7-0,8, максимально – 1,0 мг/кг массы тела, обычно не более 20-30 мг/сут. Терапевтическая доза назначается в течение 2 нед. а затем снижается по 2,5 мг один раз в 5-7 дней до полной отмены препарата, которая должна произойти не ранее, чем за 2 нед. до выписки больного из стационара. При снижении дозы преднизолона необходимо назначить нестероидные противовоспалительные средства, для продления противовоспалительного лечения до 9-12 нед. Период противовоспалительного лечения определен тем, что 95% ревматических атак купируются в период 12 недель. Отмена лечения в более ранние сроки приводит к возврату клинических и лабораторных признаков болезни, что влечет за собой удлинение атаки до 7 и более месяцев.
Преднизолон – 20-30 мг в сутки.
Триамсинолон – 12-16-20 мг в сутки.
Дексаметазон – 2-3 – 3,5 мг. Дексаметазон больше подходит для поддерживающей терапии, в остром периоде – не годится, лучше при РА.
Преднизолон – 500-700 мг.
Триамсинолон – 350-400 мг.
Дексаметазон – 50-80 мг.
Пролонгированные стероиды
Целестон – 1 раз в 3 недели В/М.
Кеналог –1 раз в 3-4 недели – В/М
Лечебный эффект глюкокортикоидов при ревматизме тем значительнее, чем выше активность процесса, поэтому больным с особенно высокой активностью (панкардит, полисерозит и т.п.) начальную дозу преднизолона увеличивают до 40-50 мг и более.
Гормонотерапию с постепенным снижением дозировки и отменой проводят, соблюдая все меры профилактики возможных осложнений (приём размельчённых таблеток после еды, запивая их большим количеством жидкости).
Эффективность назначенной дозы кортикостероидов в первые дни проще всего контролировать по значительному улучшению аппетита, уменьшению лихорадки и исчезновению суставного синдрома. Быстро происходит также процесс обратного развития ревматических поражений серозных оболочек и коней. У большинства больных в первые 2-4 недели лечения наблюдается нормализация основных лабораторных показателей активности процесса. Повышенное содержание гамма – глобулинов, а также противострептококковых антител в плазме крови – более резистентные показатели и определяются более длительно.
Нестероидные противовоспалительные средства (НПВС).
Нестероидные противовоспалительные препараты назначают при ревматическом артрите, хорее, ревмокардите легкой и средней степени тяжести, при легкой и умеренной степени активности, при подостром затяжном и латентном вариантах течения. В настоящее время предпочтение отдается препаратам из группы индолуксусной (индометацин) и арилуксусной кислот (вольтарен). Начальная доза препаратов составляет 150 мг в день в период стационарного лечения, но не меньше месяца, а затем дозу снижают в 3 раза, Возможно также назначение ацетилсалициловой кислоты в дозе 3,0-4,0 г в день или ибупрофена по 800-1200 мг в день также с последующим снижением дозы до поддерживающей. Нестероидные противовоспалительные средства обладают выраженной противовоспалительной активностью.
- Считают установленным, что морфологические признаки активности ревматического процесса длятся не менее 3-4,5 месяцев, поэтому приём НПВС продолжают в течение всего этого срока.
- Аспирин – до 4 г в сутки.
- Салициловокислый натрий 6-8 г в сутки, курс – 250-300 г.
- Салициловокислый натрий в/в 10 % р-р – 5-10 мл.
Увеличивать дозу этих препаратов нецелесообразно, так как концентрация в крови остаётся той же.
Бутадионовые производные
- Бутадион – 0,45-0,6 и не менее I месяца после выписки.
- Пиразолоновые производные
- Пирамидон 2,0-2,5 г в сутки (курс – 70-100 г)
Препараты индольного ряда.
- Индометацин (индоцид, интебан). Курсовая доза – 2500-3000 мг
После выписки продолжают лечение этим препаратом в течение 3-5 нед.
Производные фенилуксусной кислоты
- Бруфен (ибупрофен – 800-600 мг в сутки. Этот менее активный противовоспалительный препарат применяют обычно в амбулаторных условиях. Хорошо переносится больными, не переносящими салицилаты.
Производные метизиновой кислоты
- Сорипал – 600-1200 мг в сутки. Показан там же, где индоцид. Оказывает выраженное антиэкссудативное действие, антипиретический эффект.
- Дроксарил. Выпускается в таблетках и свечах. 3-6 таблеток по 250 мг – всего – 2500 мг и дополнительно – 1-2 свечи до 1000 мг.
- Бенорилат. По 600 мг в день.
- Проксен, напроксен – 750 мг в сутки.
- Пироксикам – 20 мг
- Флугалин – 2. табл.(100 мг) х 3 раза в день.
- Тилкотил – продлённого действия – по 20 мг.
- Вольтарен – 100-150 мг в сутки. Сейчас есть вольтарен продленного действия – 100 мг 1 раз в день.
В связи с введением в практику новых нестероидных противовоспалительных препаратов: диклофенака натрия (ортофен, вольтарен), ндометацина значительно превосходящих по своей эффективности ацетилсалициловую кислоту и лучше переносимых больными, значение кортикостероидов в терапии ревматизма должно быть пересмотрено. Изолированное назначение диклофенака-натрия или индометацина в полных дозах (150 мг в сутки) приводит к столь, же выраженным ближайшим и отдалённым результатам лечения острого ревматизма у взрослых, как и применение преднизолона.
В то же время, переносимость этих нестероидных средств, особенно диклофенака-натрия, оказалась значительно лучше. Наблюдается также быстрая положительная динамика внесуставных проявлений ревматизма, в том числе ревмокардита.
Однако остаётся открытым вопрос об эффективности диклофенака-натрия и индометацина при наиболее тяжёлых формах кардита (при наличии одышки в покое, кардиомегалии, экссудативного перикардита и недостаточности кровообращения), которые у взрослых практически не встречаются. Поэтому пока при .подобных формах болезни (прежде всего у детей) средством выбора является кортикостероиды в достаточно больших дозах.
Найз, мовалис, целебрекс и др. Эффективность терапии НПВС оценивают по улучшению самочувствия, стойкой нормализации температуры, исчезновению кардиалгий, восстановлению звучности тонов сердца, исчезновению шумов, нормализации лабораторных признаков активности ревматического процесса, положительной динамике ЭКГ и данных ЭХО-кардиографии.
Эти препараты являются слабыми иммунодепрессантами, стабилизаторами лизосомных мембран, за счет чего уменьшается повреждающее действие протеолитических лизосомальных ферментов. Учитывая выраженность иммунопатологических процессов и, в частности, активацию клеточно-опосредованных реакций у больных с затяжным и непрерывно-рецидивирующим течением, лучшим методом терапии в таких случаях является длительный (год и более) приём хинолиновых препаратов:
- Хлорохин (хингамин, делагил) – по 0,25 г 2раза в сутки в течение 1 месяца.
- Или плаквенил по 0,2 г 2раза в сутки. Затем по 1 табл. на ночь (в течение одного месяца).
- Эффект от применения этих средств проявляется не ранее, чем через 3-6 недель, достигает максимума через 6 месяцев непрерывного приёма.
При наличии непереносимости препаратов пенициллинового ряда используют антибиотики группы макролидов: эритромицин 0,25 4 раза в день или препараты нового поколения (азитромицин 0,5 г в первый день, далее – во 2-й – 5-й дни по 0,25 г 1 раз в день, курс – 5 дней; рокситромицин 0,15 г 2 раза в день, курс – 10 дней). Эти антибиотики высокоэффективны в отношении стрептококка и способны создавать высокую их концентрацию в очаге инфекции. Не рекомендуется лечить ОРЛ тетрациклинами, левомицетином (хлорамфениколом), фторхинолонами, сульфаниламидами, так как к этим препаратам стрептококк мало чувствителен или полностью резистентен.
В то же время необходимо помнить, что пенициллин не оказывает лечебного действия на собственно ревматический процесс, поэтому длительное и не строго обоснованное (нет очагов инфекции и нет гормональной терапии) применение пенициллина или других антибиотиков при ревматизме нерационально.
При развитии недостаточности кровообращения назначают инородные негликозидные средства (дофамин, глюкагон), малые дозы сердечных гликозидов (коргликон, строфантин, дигоксин).
- При наличии признаков застойной сердечной недостаточности у больных с выраженным кардитом они дают эффект только при одновременном применении противоревматических средств.
- Если недостаточность кровообращения развивается в связи с активным ревмокардитом, то в лечебный комплекс можно включать и стероидные гормоны, не вызывающие значительной задержки жидкости, т.е. преднизолон, метилпреднизолон или триамцинолон. Дексаметазон не показан.
Диуретики петлевые (фуросемид), тиазидные и тиазидоподобные (гидрохлортиазид, индапамид), калийсберегающие (спиронолактон, триамтерен, амилорид).
Блокаторы кальциевых каналов
Группа дигидропиридинов длительного действия (амлодипин).
Карведилол, метопролол, бисопролол.
Применение нитратов в комплексном лечении ЗСН у больных РПС в последнее время значительно снизилось из-за развития толерантности. Эти препараты также ухудшают прогноз заболевания у данной категории пациентов.
Вопрос о целесообразности применения ингибиторов АПФ больным с ревмокардитом на фоне РПС требует дальнейшего изучения. Ряд эффектов ингибиторов АПФ при ЗСН реализуется через активацию синтеза простагландинов и подавление разрушения брадикинина, также обладающего сосудорасширяющей активностью. В то же время основной механизм действия НПВП, в частности диклофенака, являющегося препаратом выбора при повторных атаках ОРЛ, связан с ингибицией синтеза простагландинов. Следовательно, совместное назначение НПВП и ингибиторов АПФ может привести к ослаблению вазодилатирующего эффекта последних.
Поливитаминные препараты и препараты, улучшающие метаболизм
- кокарбоксилаза 50-100 мг в/м и др. в течение 1 мес.
- рибоксин по 0,2 г. 2 т. 3 р. в день
- оротат калия 0,5 3 р. в день
- аспартат калия и магния 3 – 6 таблеток в сут. в 3 приема в течение 1мес.
- инозин 0,6 -1,2 г в сут в 3 приема в течение 1 мес.
- анаболические стероиды: неробол до 15-20 мг, ретаболил 1 раз в 7-10 дней
- нандролон – 1мл в/м, еженедельно (10 инъекций на курс).
- АТФ –1,0 мл 1% р-ра в/м
Эта группа препаратов улучшает метаболические процессы в миокарде, способствует активации синтеза белка, обладает антиоксидантной активностью.
Поэтому указанные средства следует сочетать с препаратами калия, в частности с панангином, либо с хлоридом или ацетатом калия.
Седативные. средства. транквилизаторы.
- При лечении больного с хореей следует иметь в виду, что антиревматические препараты не влияют непосредственно на проявления хореи.
- В подобных случаях к проводимой терапии рекомендуется присоединять люминал или транквилизаторы типа аминазина и особенно седуксена.
Возврат к привычной физической активности возможен при улучшении общего состояния пациента, не ожидая полного исчезновения хореиформных движений. Тяжелые осложнения или выраженные неврологические последствия редки
Для ведения пациентов с хореей особое значение имеют: спокойная обстановка, доброжелательное отношение окружающих, внушение больному уверенности в полном выздоровлении.
В необходимых случаях требуется принять меры, предупреждающие самоповреждение пациента в результате насильственных движений.
При непрерывно-рецидивирующем течении.
Иногда показан плазмаферез. Удаляются антитела.
- Радикальная санация очагов хронической инфекции проводится
после стихания активности ревматизма.
- Тонзиллэктомию осуществляют на фоне продолжающегося антиревматического лечения.
- Салицилаты на этот период следует заменить индометацином, чтобы устранить риск повышенной кровоточивости во время удаления миндалин.
За 3 дня до тонзиллэктомии назначают пенициллин (1500000 – 2000000 ЕД. в сутки), который отменяют лишь через 7-10 дней после операции.
Промывание лакун, КУФ
При отсутствии показаний для тонзилэктомии.
Восстановительное лечение в условиях местного специализированного реабилитационного центра (санатория) или на больничном листе (2 этап).
Этот этап необходим при переходе ревматизма в неактивную фазу.
Считается возможным даже курортное лечение больных с минимальной активностью ревматизма, правда, на фоне продолжающейся лекарственной антиревматической терапии в специализированных санаториях.
Именно на этом этапе проводят полную отмену гормонов, контролируют приём НПВС, назначают препараты, улучшающие метаболизм миокарда. С больными работают специалисты по физической а в идеале – и социальной реабилитации, что позволяет лучше подготовить их к продолжению активной жизни. С больными детьми и подростками необходимы занятия в пределах школьной программы.
Периодически проводят исследование крови, электро- и ЭХО-кардиографию (по показаниям).
Больных без пороков сердца, либо с недостаточностью митрального и, аортального клапана при отсутствии декомпенсации целесообразно направлять в Кисловодск или на Южный Берег Крыма (Ялта).
Больных с недостаточностью кровообращения I стадии, в том числе с нерезкими митральными стенозами – в Кисловодск.
Противопоказано курортное лечение при выраженных признаках активности ревматизма (II-III степени, тяжёлых комбинированных или сочетанных пороках сердца, недостаточности кровообращения II или III стадии).
Этот этап предусматривает последующее диспансерное наблюдение и профилактическое лечение больного ревматизмом.
1. Осуществление лечения, направленного на окончательную ликвидацию активного ревматического процесса.
2. Проведение симптоматической терапии нарушений кровообращения и больных с пороками сердца, решение совместно с кардиохирургом вопросов хирургической коррекции пороков.
3. Решение вопросов реабилитации, трудоспособности, трудоустройства.
4. Осуществление вторичной профилактики ревматизма, предупреждение рецидивов заболевания
До настоящего времени общепризнанным считается, что использование бициллинопрофилактики послужило одним из основных факторов, способствующих снижению рецидивов ревматизма. Но имеются убедительные данные, что снижение заболеваемости ревматизмом началось с середины 40-х годов, когда антибиотики, во всяком случае, для профилактики и лечения ревматизма, не использовались. И как тут не вспомнить некоторые работы о цикличности вспышек бета-гемолитического стрептококка группы А, возникающих периодически с интервалами в 30-50 и более лет. Не исключено, что снижение заболеваемости ревматизмом последние 40-50 лет было достигнуто не только за счет антибиотиков (в лечении и профилактике), но и вследствие естественной убыли распространенности стрептококковой инфекции и уменьшения патогенности или “ревматогенности” стрептококков.
Выглядит и сомнительным утверждение, бытовавшее в 50-70-ые годы, о плохих социальных условиях в обществе, являющихся одной из главных причин вспышек стрептококковой инфекции и, как следствие, высокой заболеваемости ревматизмом. Как можно тогда объяснить неоднократные вспышки ОРЛ в 80-х годах XX столетия в США, Японии и некоторых европейских странах с достаточно высоким социальным уровнем.
Это комплекс общегосударственных мероприятий, направленных на улучшение условий жизни населения, укрепление службы здравоохранения и повышение санитарной культуры.
Цель первичной профилактики – организация комплекса индивидуальных, общественных и общегосударственных мер, направленных на ликвидацию первичной заболеваемости ревматизмом, т.е недопущение заболеваемости ревматизмом здоровых лиц. Особо выделяют следующее:
1. Борьба со стрептококковой инфекцией:
1) Выявление носителей (обязательное бактериологическое исследование при носоглоточных инфекциях).
2) Обязательное лечение стрептококковых носоглоточных инфекций антибиотиками:
ЛС первого выбора (схемы лечения):
Взрослым в/м однократно:
Бензатин бензилпенициллин 2,4 млн. ЕД /сут.
Взрослым в/м 10 сут.:
Амоксициллин 1,5 г /сут в 3 приема в течение 10 дней;
Феноксиметилпенициллин 1,5 г /сут. в 3 приема;
Цефадроксил 1 г/сут в 2 приема
Бензатин бензилпенициллин 0,375 г/сут в 2 приема (<25 кг) или 750 мг/сут в 2 приема (>25 кг)
Детям в/м 10 сут.:
Амоксициллин 0,375 г/сут. в 3 приема (<25 кг);
Феноксиметилпенициллин 750 мг/сут. в 3 приема (>25 кг);
Цефадроксил 600 тыс. ЕД/сут. (<25 кг) 30 мг/кг в 1 прием или 1,2 млн. ЕД/сут. (>25 кг) 30 мг/кг в 1 прием
Феноксиметилпенициллин, учитывая наличие лекарственной формы в виде суспензии, рекомендуется преимущественно для лечения детей.
Бензатин бензилпенициллин целесообразно назначать при:
- возможной неисполнительности пациента в отношении внутреннего приема антибиотиков;
- наличии ОРЛ в анамнезе у больного или ближайших родственников;
- неблагоприятных социально-бытовых условиях;
- вспышках БСГА—инфекции в детских дошкольных учреждениях, школах, интернатах, училищах, воинских частях и т.п.
При непереносимости бета-лактамных антибиотиков (схемы лечения):
Взрослым внутрь 6 сут.:
Азитромицин 0,5 г/сут. в 1-е сут. затем по 0,25 г/сут. Взрослым внутрь 10 сут.:
Мидекамицин 1,2 г/сут. в 3 приема;
Рокситромицин 0,3 г/сут. в 2 приема;
Эритромицин 1,5 г/сут. в 3 приема;
Взрослым в/м 10 сут.:
Кларитромицин 0,5 г/сут. в 2 приема;
Спирамицин 6 млн. ЕД/сут. в 2 приема
Детям внутрь 5 сут.:
Азитромицин 12 мг/кг в 1 прием
Детям внутрь 10 сут.:
Мидекамицин 50 мг/кг в 2 приема;
Рокситромицин 5 мг/кг в 2 приема;
Эритромицин 40 мг/кг/сут. в 3 приема
Детям в/м 10 сут.:
Кларитромицин 15 мг/кг в 2 приема;
Спирамицин 3 млн. ЕД/сут. в 2 приема
Для эритромицина характерно наиболее частое, по сравнению с другими макролитами, развитие побочных реакций, особенно со стороны ЖКТ.
При непереносимости макролидов и бета-лактамных антибиотиков (схемы лечения):
Взрослым в/м 10 сут.:
Клиндамицин 0,6 г/сут в 4 приема;
Линкомицин 1,5 г/сут. в 3 приема
Детям в/м 10 сут.:
Клиндамицин 20 мг/кг/сут. в/м в 3 приема;
Линкомицин 30 мг/кг/сут. в/м
Антимикробная терапия рецидивирующего БГСА-тонзиллита
Взрослым внутрь 10 сут.:
Амоксициллин/клавуланат 1,875 г /с в 3 приема;
Клиндамицин 0,6 г/сут. в 4 приема
Линкомицин 1,5 г/сут. в 3 приема;
Цефуроксим/аксетил 0,5 г/сут. в 2 приема
Детям внутрь 10 сут.:
Амоксициллин/клавуланат 40 мг/кг в 3 приема;
Клиндамицин 20 мг/кг/сут. в 3 приема
Линкомицин 30 мг/кг/сут. в 3 приема;
Цефуроксим аксетил 20 мг/кг/сут. в 2 приема
3) Эти мероприятия наиболее важны и при уже развившемся ревматизме.
Если у больного в неактивной фазе ревматизма появились первые признаки предположительно стрептококковой инфекции, то помимо обязательного 10-дневного курса пенициллинотерапии, он должен в течение этого же срока принимать один из нестероидных противоревматических препаратов.
4) Санация хронических очагов стрептококковой инфекции.
2. Работа с населением.
Цель её – объяснить, что при ангинах и фарингитах необходимо показаться врачу.
3. Меры борьбы со стрептококковым окружением.
Учитывая пик заболеваемости в подростковом возрасте, высокий риск развития ревматизма в семьях больных, вспышки стрептококковой инфекции, перечисленные мероприятия приоритетно проводить в детских и подростковых коллективах (особенно закрытых) и в семьях, где есть больные ревматизмом.
Проводится иммунизация против стрептококка группы А. Синтезирована вакцина, которая будет содержать эпитопы М-протеинов «ревматогенных» штаммов стрептококков, не вступающих в перекрестную реакцию с тканевыми антигенами сердца человека. Применение такой вакцины в рамках первичной профилактики ОРЛ целесообразно, в первую очередь, у лиц с генетическими маркерами, указывающими на предрасположенность к заболеванию.
5. Меры общего повышения защитных сил организма
Спорт, закаливание, гимнастика.
По окончании курса лечения ОРЛ, сразу же начинается ее вторичная профилактика. У больного з-4 раза в году определяют антитела к сердечно-реактивному антигену. В периоды нарастания титра антител проводят бициллинопрофилактику.
1. Её проводят с целью недопущения рецидивов заболевания у лиц, уже перенесших острую ревматическую лихорадку.
2. Ей подлежат все больные, перенесшие достоверный ревматический процесс в течение последних 5 лет и по индивидуальным показаниям те, кто перенес ревматическую атаку более чем 5 лет назад.
3. Антибиотики – основа профилактики повторных ревматических атак.
В последние годы оцениваются различные антибактериальные препараты для вторичной профилактики. Перспективными антибиотиками пролонгированного действия считаются бензилпенициллины: экстенциллин (Франция), ретарпен (Австрия), пендепон (Чехия), бензатин-бензилпенициллин (США) и др. Экстенциллин в/м – 2 400 000 2р в мес. или 1 200 000 в неделю.
Наиболее эффективной лекарственной формой бензатин бензилпенициллина является экстенциллин. Исследования, проведенные в институте ревматологии РАМН и Государственном научном центре по антибиотикам, показали, что этот препарат обладает явными фармакокинетическими преимуществами в сравнении с бициллином-5 по основному параметру – длительности поддержания адекватной противострептококковой концентрации бензилпенициллина в сыворотке крови пациентов.
Взрослым и подросткам:
Бензатин бензилпенициллин, 2,4 млн. ЕД в/м один раз в 3 нед.
Детям при массе тела > 25 кг:
Бензатин бензилпенициллин, 1,2 млн. ЕД в/м один раз в 3 нед.
Детям при массе тела < 25 кг:
Бензатин – бензилпенициллин, 600 000 ЕД в/м один раз в 3 нед.
Длительность вторичной профилактики
Ее следует начинать еще в стационаре) для каждого пациента устанавливается индивидуально. Как правило, она составляет не менее 5 лет для больных, перенесших ОРЛ без кардита (артрит, хорея); более 5 лет (или пожизненно) – для больных перенесших первичную или повторную атаку ОРЛ с поражением сердца (особенно при наличии признаков формирующегося или сформированного его порока).
В России используется Бициллин-1
Бициллин-1 – 1 200 000 ЕД 1 раз в 7 дней
В настоящее время препарат бициллин-5 (смесь 1,2 млн. ЕД бензатин – бензилпенициллина и 300 тыс. ЕД новокаиновой соли бензилпенициллина) рассматривается как несоответствующий фармакокинетическим требованиям, предъявляемым к превентивным препаратам, и не является приемлемым для проведения полноценной вторичной профилактики ОРЛ.
Длительность вторичной профилактики – не менее 5 лет после достоверной последней ревматической атаки, если ОРЛ протекала с кардитом и 3 года, если ОРЛ протекала без поражения сердца при отсутствии у пациента очагов хронической инфекции. Сроки бициллинопрофилактики обусловлены тем, что 75% повторных ОРЛ возникают в первые 3 года и 92% – в первые 5 лет от начала заболевания. В более отдаленные сроки риск возникновения нового эпизода ОРЛ невелик.
Бициллинопрофилактика должна проводиться круглогодично, без перерывов. Сезонная бициллинопрофилактика (в весенне-осенний период) не позволяет предотвратить рецидивы ОРЛ в промежутках между курсами профилактической терапии. Эффективность сезонной бициллинопрофилактики в 10 раз ниже, чем круглогодичной.
В.А Насонова считает, что если в течение 5 лет нет никаких обострений, рецидива ревматизма то профилактика может быть прекращена.
Старше 25 лет бициллинопрофилактику не надо продолжать, так как длительное потребление лекарств ведет к изменению в почках, снижаются иммунобиологические свойства. Беда в том, что бициллин-5 не оказывает профилактики. Он потерял свою эффективность, так как изменилась активность белка.
В.А. Насонова: «Бьемся 5 лет, только сейчас удалось его снять с бициллинопрофилактики. Это так, но хотя бы не будет иллюзий, что проводим профилактику. Экстенциллин 2,4 млн 1 раз в 3 нед.»
Рекомендации ВОЗ по вторичной профилактике ревматизма
Имеют некоторые отличия. Эксперты ВОЗ выделяют 2 вида вторичной профилактики ревматизма: внутримышечную и пероральную. Первая проводится с помощью бициллина по 1 200 000 ЕД взрослым и детям с массой тела более 30 кг, а детям с массой тела менее 30 кг – по 600 000 ЕД 1 раз в 3 недели. Пероральная профилактика ревматизма проводится феноксиметилпенициллином по 250 мг 2 раза в сутки. При непереносимости пенициллина рекомендуется профилактический прием эритромицина по 250 мг 2 раза в сутки.
По рекомендации ВОЗ длительность вторичной профилактики зависит от клинических особенностей течения ОРЛ и возраста пациента. Если ОРЛ протекала без кардита, то вторичная профилактика должна проводиться не менее 5 лет, но прекращаться не ранее, чем по достижении пациентом 18 лет, иногда дольше. Больным, перенесшим ОРЛ с кардитом, проводить профилактику надо по крайней мере до 25 летнего возраста. Больным с клапанным пороком сердца и тем, кому выполнялась хирургическая коррекция порока сердца, эксперты ВОЗ рекомендуют проводить вторичную профилактику ревматизма в течение всей жизни.
В соответствии с данными экспертов Американской кардиологической ассоциации, все больные с РПС входят в категорию умеренного риска развития инфекционного эндокардита.
В условиях вторичной профилактики обязательным является проведение текущей профилактики ревматизма.
Текущая профилактика заключается в назначении антибактериальных препаратов, к которым чувствителен стрептококк, всем больным, перенесшим ОРЛ, при интеркуррентных инфекционных заболеваниях и малых операциях (экстракция зуба, аборт, тонзиллектомия и др.) в терапевтических дозах. При малых операциях пероральный прием антибиотиков может быть заменен парентеральным введением бензилпенициллина в течение 5 дней с последующим введением бициллина-1 в стандартных дозах.
При манипуляциях на полости рта, пищеводе, дыхательных путях Стандартная схема:
Взрослым внутрь за 1 час до процедуры:
Детям до 12 лет внутрь за 1 час до процедуры:
Амоксициллин 950 мг/кг
- При невозможности внутреннего приема:
Взрослым в/в или в/м за 30 мин. до процедуры:
Детям до 12 лет в/в или в/м за 30 мин. до процедуры:
Ампициллин 50 мг/кг.
- При аллергии к пенициллину
Взрослым внутрь за 1 час до процедуры:
Азитромицин 500 мг;
Кларитромицин 500 мг;
Клиндамицин 600 мг;
Цефадроксил 2 г;
Детям до 12 лет внутрь за 1 час до процедуры:
Азитромицин 15 мг/кг;
Кларитромицин 15 мг/кг;
Клиндамицин 20 мг/кг;
Цефадроксил 50 мг/кг;
Цефалексин 50 мг/кг.
При аллергии к пенициллинам и невозможности внутреннего приема
Взрослым за 30 мин. до процедуры:
Клиндамицин в/в 600 мг;
Цефазолин в/м или в/в 1 г
Детям до 12 лет за 30 мин. до процедуры:
Клиндамицин в/в 20 мг/кг;
Цефазолин в/м или в/в 25 мг/кг
При манипуляциях на желудочно-кишечном и урогенитальном трактах Стандартная схема.
Амоксициллин 2 г. внутрь за 1 час до процедуры;
Ампициллин 2 г в/м или в/в, введение закончить за 30 мин. до процедуры Детям до 12 лет:
Амоксициллин 50 мг/кг внутрь за 1 час до процедуры;
Ампициллин 50 мг/кг в/м или в/в, введение закончить за 30 мин. до процедуры.
При аллергии к пенициллинам
Взрослым в/в в течение 1—2 часов, введение закончить за 30 мин. до процедуры:
Детям до 12 лет в/в в течение 1—2 часов, введение закончить за 30 мин. до процедуры:
Ванкомицин 20 мг /кг
Как я уже сказала, целью текущей профилактики является не только предотвращение рецидива ОРЛ, но предотвращение развития инфекционного эндокардита.
Беременные, больные ревматизмом ,
С первых недель наблюдаются совместно ревматологом и акушером-гинекологом, которые решают вопрос о сохранении или прерывании беременности и бициллинопрофилактике.
При беременности у женщин, перенесших ОРЛ, проводящаяся бициллинопрофилактика не отменяется. Но если к моменту беременности бициллинопрофилактика была уже прекращена, то ее возобновление при необходимости возможно с 10-12 –недельного срока беременности.
Определенные опасения при проведении бициллинопрофилактики возникают в связи с возможностью аллергических реакций. Обязательным условием является введение бициллина в процедурной, хорошо оснащённой для проведения противошоковых мероприятий. Обучение персонала быстро и чётко их осуществлять.
Больным хроническими вариантами течения ревматизма и хронической недостаточностью кровообращения необходима длительная комплексная терапия – антибактериальная, противовоспалительная и аминохинолиновая, которая играет роль вторичной профилактики обострений.
На протяжении второй половины XX века не прекращались попытки получить стрептококковую вакцину. Последние достижения в области молекулярной биологии, позволившие иметь ценную дополнительную информацию о стрептококке группы А, дают основание надеяться на создание в будущем эффективной вакцины против ОРЛ.
К основным осложнениям ревматизма относят:
- Формирование клапанного порока сердца.
- Развитие застойной сердечной недостаточности.
- Нарушение ритма.
- Тромбоэмболии (особенно при появлении фибрилляции предсердий).
- Возникновение септического эндокардита.
Прогноз заболевания определяют эффективность лечения первичного ревмокардита и наличие осложнений.
Пребывание на больничном листе
- Острая ревматическая лихорадка
- Без поражения сердца – 30-50 дней
- С поражением сердца:
I ст. активности – 40-45 дней
II ст. активности – 50-65 дней
III ст. активности – 85-110 дней
- Хорея – 35-40 дней
- Хроническая ревматическая болезнь сердца.
