Глава VI. Хирургическое лечение хронического панкреатита
Вопрос о хирургическом лечении хронического панкреатита часто нельзя решить однозначно. К операции следует склоняться лишь в тех случаях, когда настойчивая и все* сторонняя консервативная терапия, проводимая в течение нескольких лет, остается неэффективной.
Характер оперативного вмешательства зависит от ведущего этиологического фактора заболевания, его стадии и изменений гепатобилиарной или гастроэнтеральной систем, патологию которых можно корригировать хирургическим путем.
Хирургическое лечение хронического панкреатита показано в первую очередь при осложненных формах заболевания, сопровождающихся обтурационной желтухой (индуративный и псевдотуморозный панкреатит), болевых формах панкреатита, когда длительное консервативное лечение неэффективно, при вирсунголитиазе и исходе хронического панкреатита в кисту. Относительные показания к операции могут возникнуть при тех формах заболевания, которые развиваются на фоне язвенной болезни, хронического холецистита, гастрита, колита и пр.
Операция не показана при сопутствующем сахарном диабете, при так называемых безболевых, латентно протекающих формах заболевания, а также у пожилых людей с выраженными метаболическими расстройствами и декомпенсированными механизмами адаптации.
При назначении хирургического лечения необходимо помнить о его нередко ограниченных возможностях. Операция, предпринимаемая по поводу хронического панкреатита, не должна быть и опаснее самого заболевания. А это в первую очередь требует оптимального объема операции применительно к каждому конкретному случаю с учетом индивидуальных особенностей больного.
Оперативное вмешательство по поводу хронического панкреатита должно преследовать три основные цели: устранение первопричины заболевания, снятие болевого синдрома и обеспечение нормального оттока в кишечник панкреатического сока и желчи. Только при хроническом панкреатите с исходом в кисту можно говорить об устранении «следствия» заболевания, т. е. самой кисты.
В отечественной и зарубежной литературе были неоднократные попытки классифицировать методы хирургического вмешательства при хроническом панкреатите и свести их в систему, которую можно рекомендовать практическим хирургам для повседневного пользования.
Л. С. Минкин (1930) предлагал делить все виды операций на прямые (резекция поджелудочной железы, капсулотомия) и непрямые (наружный и внутренний дренаж желчных путей). Warren (1959) также разделяет методы хирургического лечения панкреатита на две группы: непрямые (операции на желчных путях, желудочно-кишечном тракте и невротомии) и прямые (дренаж кист, литотомия, наложение панкреато-кишечных анастомозов и резекция железы).
Blumenthal.H Probstein (1959) делят оперативные вмешательства при хроническом панкреатите на вмешательства, направленные на устранение заболеваний желчных путей: вмешательства, позволяющие произвести внутренний или наружный дренаж желчного протока; операции на поджелудочной железе; вмешательства, имеющие целью снизить секрецию поджелудочной железы; вмешательства, устраняющие боль.
Sarlies и Mercadier (1960) в хирургии хронического панкреатита уделяют особое внимание операциям на желчных путях.
Для выбора оперативного вмешательства Hess. (1961) делит все панкреатиты на три группы: 1) хронический холецистопанкреатит (20%), протекающий с хроническим холециститом или холангитом, с камнями или без них. Удаление желчного пузыря или камней из протоков излечивает и панкреатит; 2) ретенционный панкреатит (35%), протекающий со стенозирующим папиллитом. Операция сводится к устранению препятствия оттоку панкреатического сока; 3) первичный панкреатит (40%), при котором нет ни заболеваний желчных путей, ни препятствия в выводных протоках. Возможны только паллиативные операции на нервной системе.
О. Б. Порембский (1965) относит к непрямым оперативным вмешательствам при панкреатитах операции на желчных путях, желудке и нервах, а к прямым—внутренний и наружный дренаж панкреатических кист, литотомию, анастомозы поджелудочной железы и ее протоков с другими органами желудочно-кишечного тракта.
М. А. Трунин (1969) предлагает различать операции на поджелудочной железе (резекции, панкреато-кишечных анастомозы, наружный и внутренний дренаж кисты, панкреатэктомии и вирсунголитотомии); операции на органах, связанных с поджелудочной железой (холецистэктомии, холедохотомии, билиодигестивные анастомозы); и операции на вегетативной нервной системе (варианты ваготомии и симпатэктомий).
Мы считаем целесообразным выделить четыре группы операций при хроническом панкреатите.
Классификация операции при хроническом панкреатите
A. Операции на поджелудочной железе:
резекция поджелудочной железы;
панкреато-дуоденальная резекция;
панкреатэктомия;
панкреато-кишечный анастомоз;
внутренний дренаж панкреатической кисты;
вирсунголитотомия.
Б. Операции на билиарном тракте: холецистэктомии;
наружный дренаж желчных путей; билиодигестивные анастомозы:
а) с двенадцатиперстной кишкой;
б) с тощей кишкой;
папиллотомия, сфинктеротомия.
B. Операции на желудке и двенадцатиперстной кишке:
гастроэнтероанастомоз;
резекции желудка; дуоденоеюноанастомоз. Г. Операции на вегатативной нервной системе: торако-люмбальная симпатэктомия; резекции солнечного сплетения; постганглионарная невротомия; маргинальная невротомия;
селективная невротомия ветвей чревной артерии; ваготомия.
Как видно из приведенной схемы (классификации) оперативных вмешательств, хирургическое лечение хронического панкреатита отличается известной пестротой, которую можно объяснить различиями в патогенезе заболевания.
Мы располагаем опытом 366 операций такого рода, которые были выполнены 277 женщинам и 89 мужчинам в возрасте от 20 до 70 лет. Наибольшее число больных были в возрасте от 40 до 60 лет.
В предыдущей главе мы уже говорили о том, что всем больным, поступающим в стационар, проводилось вначале консервативное лечение. Основными параметрами, определяющими показания к оперативному лечению панкреатита, мы считали стадию воспалительного процесса, выраженность болевого синдрома, наличие желтухи, отсутствие эффекта от консервативного лечения, состояние органов, заболевание которых вызывает панкреатит, общее состояние и отношение больного к операции.
Перед операцией немаловажное значение имеет подготовка психики больного. Дело в том, что хронический панкреатит протекает на фоне постоянного болевого синдрома. Боли настолько изнуряют больных, что через 3—4 года у них резко изменяется нейропсихический статус, хотя специалисты подчас и не находят при этом каких-либо выраженных заболеваний нервной системы. Хирургу непременно следует учитывать это обстоятельство при подготовке больных к операции и проводить комплексную терапию, включая назначения, сделанные невропатологом, терапевтом, анестезиологом-реаниматологом. Только при направленном специальном лечении удается снять нежелательный ипохондрический фон, что составляет существенную часть предоперационной подготовки.
Необходимо также создать у больного уверенность в благоприятном исходе операции. Вместе с тем не следует скрывать серьезности предстоящего вмешательства и возможности неполной ликвидации симптомов заболевания. Беседа врача, чуткое отношение и забота медицинского персонала, общение с лицами, благополучно перенесшими подобную операцию, преображают больных: у них появляется бодрость и исключительная настойчивость в борьбе за жизнь, они ждут операции, как единственного спасительного средства, идут на нее охотно и уверенно.
При хроническом панкреатите в большинстве случаев наблюдается истощение, гиповитаминоз, гипопротеинемия, поэтому в предоперационном периоде больным показано введение плазмы, аминопептида, гидролизина, иногда жидкости в виде физиологического раствора и 5% раствора глюкозы под контролем содержания белков в крови. Переливание крови перед операцией необходимо тогда, когда не удается медикаментозными средствами увеличить протромбиновый индекс, повысить уровень белка, гемоглобин.
Инсулин следует вводить при скрытом диабете, при отклонении от нормы кривой сахарной нагрузки. При этом следует учитывать, что инсулин стимулирует секреторную деятельность поджелудочной железы, а это при закрытых протоках приводит к набуханию железы и усилению болей (А. А. Шалимов, 1964).
При поражении головки железы и сдавлении панкреатических протоков в первую очередь страдает питание и происходит нарушение метаболизма вследствие выпадения внешней секреции поджелудочной железы, причем нарушение функции липазы и трипсина не полностью компенсируется ферментами кишечника. Жир и белок не усваиваются; падает масса тела больных. Поэтому им необходимо давать легко усваиваемую пищу, с минимумом жиров и ограниченным количеством белков.
При желтухе в связи с отсутствием в кишечнике желчи, превращающей нерастворимые соединения витаминов в растворимые, у больных развивается гипо- и даже авитаминоз. Для его устранения необходимо вводить различные витамины внутрь или парентерально: витамин Вi (5% раствор по 1 мл, 10—15 инъекций), витамин С (5% раствор аскорбиновой кислоты по 1 мл, 10—15 инъекций), витамин D внутрь, витамин Вб (5% раствор по 1—2 мл внутримышечно 1—2 раза в день в течение 10— 15 дней), витамин Bi2 (0,05% раствор внутримышечно по 1 мл ежедневно в течение 3—5 дней).
При длительной желтухе большую роль в предоперационной подготовке играют метионин (по 0,5 г 3 раза в день, 10 дней), липокаин (по 0,3 г 3 раза в день, 10 дней) и сирепар (по 5 мл 1 раз в день внутривенно 7 дней). Следует рекомендовать творог (до 300 г в день), обладающий выраженным липотропным свойством.
Операции выполняли под наркозом, с премедикацией, которую начинали накануне. При этом использовали успокаивающие, седативные и снотворные средства в составе специальных ректальных свечей. За полчаса до операции больным вводили 1 мл 0,1% раствора сульфата атропина и промедол (1% по 1 мл). Для вводного наркоза применяли седуксен, гексенал, пентазацин, для получения мышечной релаксации — листенон, тубарин, тубокурарин в обычных дозах. Для обезболивания использовали эндотрахеальный наркоз закисью азота с кислородом с добавлением фторотана, эфира или хлороформа. В некоторых случаях фракционно вводили анальгетик фортрал (фентапил), позволяющий значительно сократить расход основного ингаляционного наркотика, например фторотана, и даже иногда вообще обойтись без него. Во время операции на поджелудочной железе, расположенной вблизи солнечного сплетения, могут наступить коллаптоидные состояния, особенно в момент пересечения постганглионарных нервных волокон при невротомии. Это необходимо учитывать и быть готовым к возможному снижению артериального давления. Для предупреждения этого необходимо поддерживать достаточно глубокий наркоз.
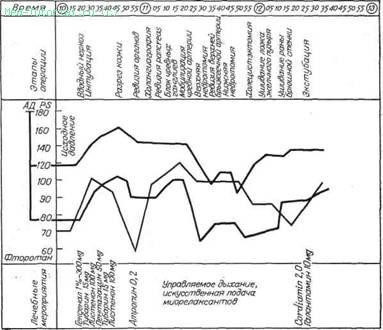
Рис. 37. Наркозная карта больной С, 50 лет, оперированной по поводу хронического панкреатита.
На рис. 37 приведена наркозная карта больной С, 50 лет, которая была оперирована по поводу хронического панкреатита. Как видно из данных наркозной карты, момент выделения чревного ствола, печеночной и селезеночной артерий, а также правого и левого чревных ганглиев сопровождался падением артериального давления и учащением пульса. После невротомии артериальное давление постепенно вернулось к исходному уровню.
Операции на поджелудочной железе
Операции на поджелудочной железе при хроническом панкреатите преследуют минимум две основные цели: создание беспрепятственного оттока панкреатического сока и удаление пораженной части железы.
Наиболее оправданной операцией, по-видимому, следует считать резекцию поджелудочной железы. В этой операции нашел предельно ясное выражение основной принцип хирургии — удалять нежизнеспособную часть пораженного органа.
Jordan, Grossman считают, что к резекции поджелудочной железы надо прибегать при выраженной дисфункции последней, когда есть типичный анамнез хронического рецидивирующего болевого панкреатита, а также прогрессирующее исхудание, выраженная стеаторея, кальцификация железы, замедленная реакция на секретин, диабет.
Многие хирурги считают, что удалять всю или часть поджелудочной железы следует в тех случаях, когда больной не получил облегчения от разгрузочных или паллиативных операций и продолжает страдать сильнее прежнего.
Следует подчеркнуть, что при хроническом панкреатите вследствие спаек и перипроцесса резекцию осуществить труднее, чем при раке; летальность после нее доходит до 30—40%. Вместе с тем левосторонняя резекция железы с оставлением селезенки отличается относительно благоприятным послеоперационным течением и удовлетворительными отдаленными результатами. Так, все 9 больных, которым М. А. Трунин (1973) произвел такую операцию, чувствуют себя удовлетворительно, продолжают выполнять прежнюю работу. В то же время из 6 больных после левосторонней резекции поджелудочной железы вместе с селезенкой хороший отдаленный результат отмечался у 4. Остальных больных автор оперировал повторно.
Мы произвели резекцию поджелудочной железы 15 больным хроническим индуративным панкреатитом с преимущественной локализацией дегенеративного процесса в области хвоста железы. В 7 случаях резекция проходила без удаления селезенки. Наблюдения за этими больными показали, что болевые приступы у них стали реже и слабее, однако полного излечения не наступило.
Больной Д. 23 лет, произведено удаление кистозно измененной опухоли тела и хвоста железы, оказавшейся доброкачественной цистаденомой; другой больной, А. 39 лет, при этом пришлось удалить также селезенку, интимно спаянную с поджелудочной железой.
Так как при каудальной резекции поджелудочной железы нередко приходится прибегать к спленэктомии, многие хирурги стали использовать поперечную панкреатосностомию (3. Т. Сенчилло-Явербаум, Partington, Ro-chelle, Carnell e. a. Gampanele и Gardner, S'ilen V. e. a. H. P. Зеленин). Doubilet и Mullholand производят эту операцию без резекции поджелудочной железы, пересаживая в петлю кишки оба конца рассеченной железы.
При тотальных формах дегенерации и рубцового перерождения панкреатической паренхимы может возникнуть вопрос о панкреатэктомии. Впервые в 1946 г. Glaget выполнил панкреатэктомию при хроническом панкреатите. В 1948 г. в клинике Мауо было произведено уже 49 панкреатэктомии, из них 8 по поводу хронического панкреатита.
По данным Howard (1960), из 24 больных хроническим панкреатитом, перенесших панкреатэктомию, в живых осталось только 12, из которых у 9 после операции прошло меньше года. Лишь 1 больной прожил после этой операции 8 лет. Эти больные являются тяжелыми инвалидами, вынужденными постоянно принимать инсулин, к которому они очень чувствительны. Малейшая ошибка в дозировке препарата может быть причиной тяжелой комы.
На наш взгляд, панкреатэктомии применима лишь при раке головки и тела железы. Только в этих случаях риск операции оправдан. Помимо опасности самого вмешательства, эти больные вынуждены всю жизнь принимать гормоны поджелудочной железы, что ставит под большое сомнение целесообразность панкреатэктомии при хроническом панкреатите.
Резекция железы неизбежно связана с обеспечением оттока панкреатического сока в кишечник, что лучше всего достигается наложением различных панкреатодигестивных анастомозов. Эта операция становится единственно возможной при рубцово-дегенеративном процессе в области головки поджелудочной железы, при стриктуре вирсунгова протока либо при вирсунголитиазе, когда возникает полный панкреатический блок.
При этом виде поражения предложено три вида операций: продольное рассечение железы и вирсунгова протока со вскрытием всех каналов, ликвидацией стриктур и удалением камней; каудалъная резекция железы (при левостороннем вирсунголитиазе); панкреодуоденальная резекция.
После продольного рассечения железы необходимо наложение панкреатоеюноанастомоза — операция технически сложная и дающая до сих пор высокий процент летальности вследствие слабой жизнеспособности анастомоза в условиях самоактивации ферментов. Однако экспериментальные данные А. А. Гладченко (1955) показали, что после панкреатоеюноанастомоза в кишечном содержимом есть панкреатические ферменты. Подобные же данные были получены в экспериментах В. Д. Келемана (1958) и Л. М. Евтушенко (1964), что свидетельствует о целесообразности данного вмешательства.
При множественных стриктурах панкреатического протока и при удовлетворительной функции поджелудочной железы Silen с соавт. (1955) прибегли к наложению продольного панкреатоеюноанастомоза у 15 больных, не потеряв ни одного.
Те же причины (множественные стриктуры панкреатического протока внутри железы, почти до ее шейки) побудили и Puestow (1958) пропагандировать завершение каудальной резекции железы латеролатеральным продольным вирсунгоеюноанастомозом.
В 1965 г. Puestow сообщил о 100 панкреатоеюностомиях, в том числе и о продольной панкреатоеюностомии, причем, по данным автора, более 75% пациентов были избавлены от болей и у них восстановилась функция поджелудочной железы. Продольную панкреатоеюностомию С. В. Puestow рекомендует производить при толстой и короткой железе, подходя к ней через вскрытую желудочноободочную связку. Затем пересекают тощую кишку на 25—35 см ниже трейцевой связки. Дистальный конец кишки проводят через брыжейку поперечноободочной кишки и накладывают анастомоз бок в бок между этим отрезком кишки и вскрытым панкреатическим протоком. Проксимальный конец кишки анастомозируют с дистальным (рис. 38).
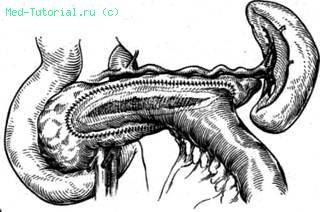
Рис. 38. Латеральный панкреатоеюноанастомоз по Puestow I.
Для достижения успеха при продольной панкреатоеюностомии, по наблюдениям Puestow, имеют значение следующие моменты: все изолированные карманы внутри поджелудочной железы должны быть вскрыты и дренированы; никогда не следует анастомозировать проток железы с не выключенной из пищеварения петлей тощей кишки, а надо использовать изолированный отрезок кишки; не следует подшивать слизистую оболочку кишки к протоку железы, а анастомозировать серозную оболочку кишки с наружной поверхностью железы; изолированный отрезок кишки следует проводить позади поперечно-ободочной кишки.
При обнаружении непроходимости панкреатического протока в области головки поджелудочной железы или перешейка показана панкреатоеюиостомия по Cattel или Шалимову (рис. 39).
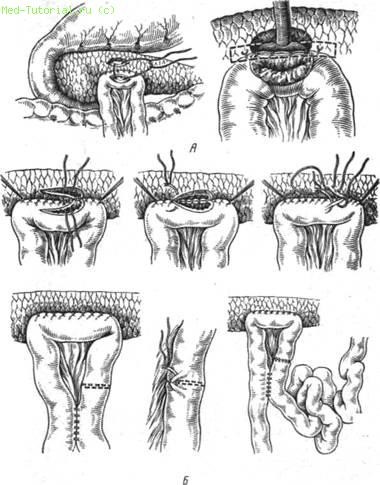
Рис. 39. Варианты панкреато-кишечных соустий. А — по Cattel; В — по А. А. Шалимову.
Как видно из рисунка, методика панкреатоеюностомии по Cattel заключается в наложении анастомоза между тонкой кишкой и вирсунговым протоком, рассеченным не на всю длину, а лишь на протяжении 2 см. А. А. Шалимов выполняет этот анастомоз по типу широкого соустья, прошивая приводящую петлю кишки аппаратом УКЛ.
По-видимому, более оправдана операция каудальной панкреатоеюностомии, выполняемая в различных модификациях (Duvall, Puestow, А. А. Шалимов). Методика операции по Puestow состоит в частичной резекции и рассечении хвоста железы вдоль. Затем рассеченную левую половину железы инвагинируют в изолированную по Ру петлю тощей кишки (рис. 40). Анастомоз накладывают позадиободочно.
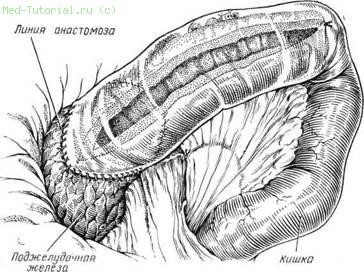
Рис. 40. Дистальный панкреатоеюноанастомоз.
Многие хирурги высказываются против наложения панкреатодигестивного анастомоза, считая его сложным и
рискованным (Longmire, Jordan, Briggs, Partington). По данным Partington и Rochellae, из 7 подобных операций в 3 случаях наблюдался полный возврат всех прежних признаков болезни в ближайшее время.
По данным О. Б. Порембского, наложение панкреатоеюноанастомоза сопряжено с большими опасностями в связи с развитием некротических процессов в поджелудочной железе. Обе оперированные им больные, которым был наложен подобный анастомоз, умерли от перитонита.
По данным Leger с соавт. из 6 больных, которым был наложен вирсунгоеюноанастомоз, у 4 через год после операции была обнаружена полная непроходимость этого анастомоза.
Следовательно, панкреатодигестивные анастомозы при хроническом панкреатите не только являются сложным и опасным вмешательством, но и не всегда обеспечивают поступление ферментов поджелудочной железы в желудочно-кишечный тракт. Эти анастомозы можно накладывать только в том случае, когда имеются неустранимые стриктуры вирсунгова протока в области головки поджелудочной железы, что позволяет сохранить внешнесекреторную функцию поджелудочной железы.
Мы выполнили 20 подобных операций на поджелудочной железе с вполне удовлетворительными результатами и предпочитаем ее каудальной резекции.
По нашим наблюдениям, жестокий болевой синдром, вызванный стриктурами вирсунгова протока, протекает особенно тяжело при сочетании последних с недостаточностью сфинктера Одди, когда не устранена основная причина заболевания — стойкий энтеральный рефлюкс.
У больной Б. 32 лет, в течение 5 лет страдавшей хроническим панкреатитом, при типичной хронической картине заболевания с выраженным нейровегетативным синдромом имелись значительные изменения внешней и внутренней секреции поджелудочной железы. В связи с болевой формой хронического рецидивирующего панкреатита была произведена операция, во время которой выявлена недостаточность сфинктера Одди; манометрическое давление в желчном пузыре было равно 80 мм вод. ст. (при норме 220— 270 мм), давление в холедохе 70 мм вод. ст. Поджелудочная железа оказалась увеличенной в размерах, местами дольки ее склерозированы, особенно в области головки и хвоста. Камней в желчных путях обнаружено не было. Произведена маргинальная невротомия поджелудочной железы. Однако операция не привела к ожидаемому результату: боли не стихли, больная продолжала худеть, у нее возникли явления ипохондрии и апатии. В связи с этим спустя год она была оперирована повторно. На операции поджелудочная железа утолщена, уплотнена, особенно в области головки и тела, диагностирован индуративный панкреатит. После мобилизации левой половины железы произведена резекция хвоста и наложен каудалъный панкреато-кишечный анастомоз с изолированной по Ру петлей тощей кишки.
Однако и эта операция не излечила больную полностью. Выписавшись из клиники, она продолжала чувствовать себя плохо, не смогла приступить к работе, осталась на инвалидности.
Трудно объяснить причину таких неудач. По-видимому, прав О. Б. Порембский, видя причину их в выраженных метаболических расстройствах, Присущих хроническому панкреатиту. Эти последние в свою очередь глубоко поражают нервную систему, резко нарушают процессы обмена веществ, способствуют тяжелой дистрофии, когда возможности хирургии крайне ограничены.
В случаях исхода хронического панкреатита в кисту мы накладываем обычно цистоеюноанастомоз с межкишечным анастомозом. При пункции кисты поджелудочной железы, как правило, получаем прозрачную жидкость от 300 до 1500 мл и больше. Перед операцией больные обычно имеют длительный анамнез, говорящий о хроническом воспалительном процессе в поджелудочной железе.
У больной М. 35 лет, страдавшей несколько лет хроническим панкреатитом, во время операции было установлено, что поджелудочная железа находится в состоянии хронического рубцово-склеротического процесса с обтурацией вирсунгова протока. В области тела железы последний был расширен в виде кисты, выстланной эпителием, имел размер 18X14X12 см и содержал около 1500 мл желтоватой жидкости. Наложен цистоэнтероанастомоз с межкишечным соустьем.
При гистологическом исследовании обнаружена ретенционная киста из выводящих путей поджелудочной железы вследствие их обтурации рубцовой тканью».
Ряд больных были оперированы по поводу хронического панкреатита, развившегося на фоне язвенной болезни. Этим больным произвели резекцию желудка с клиновидной резекцией поджелудочной железы, в связи с пенетрацией язвы и реактивным панкреатитом.
В ряде случаев с целью улучшения кровоснабжения поджелудочной железы при хроническом панкреатите пытались подшивать к ней сальник (оментопанкреатопексия).
У больного М. 52 лет, при ревизии брюшной полости после лапаротомии по поводу хронического панкреатита к поджелудочной железе была подшита большая прядь сальника на ножке в надежде на улучшение кровообращения в паренхиме железы, пораженной фиброзом.
Эта операция первое время как будто дала ожидаемый результат, но спустя год боли возобновились с прежней силой. По-видимому, операции такого рода рекомендовать не следует.
Говоря о прямых операциях на поджелудочной железе, нельзя не сказать о биопсии ткани железы, которую нередко делают с дифференциально-диагностической целью.
Различают два вида биопсий: ножевую и пункционную с помощью различных игл. Ножевую биопсию стали применять сравнительно давно (Probstein е. а. 1950).
Однако накопление опыта привело к разочарованию, так как, вероятно, в срез попадают более поверхностные участки неизмененной панкреатической ткани (Б. А. Петров, 1958; А. В. Смирнов, 1960; 1961; В. И. Пужайло, 1963).
Кроме того, было отмечено, что, например, при опухолях поджелудочной железы, достоверность ножевой биопсии снижается из-за воспалительного валика, окружающего опухоль. В подобных случаях необходимо брать кусочки из нескольких мест железы и с разной глубины, что нередко сопровождается осложнениями. Наиболее частыми из них являются кровотечения, образование свищей и перитонит (В. И. Пужайло, 1963; Kaufman, 1955; Spiut e. a. 1957; Bojden, 1957, и др.). Для предупреждения развития свищей и перитонита Mallet-Guy в 1957 г. рекомендовал дренировать сальниковую сумку.
Большое применение нашла игольная — пункционная биопсия (Howard, 1951; Grile, 1952; Ackerman, 1955; Cote, 1959; Rankin, 1964, и др.)- В нашей стране ее применяют А. Ф. Лобко (1965), М. А. Трунин (1965) и др.
Пункционная биопсия имеет ряд преимуществ. С ее помощью можно получить ткань из глубины уплотненного участка или из нескольких мест по усмотрению хирурга. У А. Ф. Лобко, например, в результате пункционной биопсии и исследования биопсированных участков железы диагноз изменился у 9 из 25 оперированных больных. Пункционную биопсию поджелудочной железы обычно делают теми же иглами, что и биопсию печени (А. Ф. Блюгер и М. Н. Синельникова, 1962; Silverman, 1938; Ferry, 1949; Mengini, 1958).
Представляет интерес методика биопсии, предложенная ленинградским анатомом и хирургом И. Ф. Крутиковой. Автор путем многолетних исследований установил своеобразную структуру клубочка поджелудочной железы, имеющего свою сосудистую ножку и в известной степени отделенного от соседнего клубочка тонкой перегородкой (рис. 41).
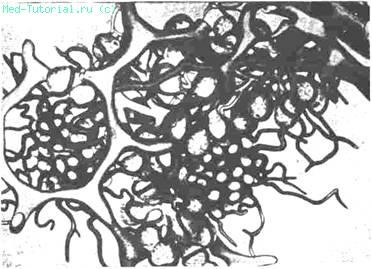
Рис. 41. Строение «клубочка» отдельной дольки поджелудочной железы (по И. Ф. Крутиковой).
Дольку выделяют тупо, в пределах междольковой бороздки и промежутка с изолированной перевязкой дольковой ножкой. При этих условиях выделенная долька железы полностью сохраняет свою структуру, а секреторные ходы соседних долек остаются ненарушенными. Однако изолированное выделение дольки возможно при мало измененной мягкой поджелудочной железе, когда биопсии обычно не требуется. При фиброзе и склерозе поджелудочной железы выделение дольки в большинстве случаев невозможно, а иногда просто опасно. Примером может служить следующее наблюдение.
Больной П. 36 лет, был оперирован в клинике в 1966 г. по поводу хронического холецистопанкреатита. Во время операции был удален деформированный желчный пузырь. Поджелудочная железа была каменистой плотности, бугристая, что послужило ^основанием заподозрить рак поджелудочной железы. Оснований для наложения билиодигестивного анастомоза не было. Через 10 дней больной был выписан. Спустя 4 года он вновь был подвергнут оперативному вмешательству по поводу тянущих болей в области правого подреберья, слабости, снижения трудоспособности. Во время повторной операции была удалена длинная культя пузырного протока и взята биопсия путем удаления изолированной дольки поджелудочной железы. В послеоперационном периоде развился перитонит, по поводу чего больной был оперирован в третий раз (ревизия и дренаж брюшной полости). После биопсии около 3 мес не заживал панкреатический свищ. Он закрылся после отторжения участка поджелудочной железы размером 7X4 см. Больной выздоровел, но провел в клинике 121 день.
В связи с этим мы предпочитаем пункционную биопсию поджелудочной железы. Показанием к ней, как правило, служит псевдотуморозная форма хронического панкреатита, когда воспалительно-дегенеративный процесс в ткани поджелудочной железы напоминает раковое поражение. При этом гистологически были найдены разные степени хронического воспаления поджелудочной железы — от очагового фиброза стромы до диффузного разрастания грануляционной ткани с явлениями рубцевания панкреатической паренхимы. Тем не менее и пункционную биопсию поджелудочной железы мы считаем небезопасным мероприятием, нередко дающим тяжелые осложнения в виде свищей, перитонита, острого панкреонекроза и т. п. Обращает на себя внимание довольно длительное пребывание в стационаре больных, перенесших биопсию поджелудочной железы. В среднем, по нашим данным, оно составляло 55 дней. Как правило, это объяснялось тяжелым послеоперационным периодом.
У больного Н. 49 лет, поступившего в клинику с синдромом желтухи, истинная картина заболевания оставалась Ц| Совсем ясной. Во время операции в области поджелудочной женены было обнаружено плотное, как камень, образование, сдавившие желчные протоки. Пункционная биопсия поджелудочной желппы исключила рак и больному наложен разгрузочный холецисто-дуодоиоанастомоз. В послеоперационном периоде развился перито-11И1, тяжелая печеночная кома и вторичная сердечная недостаточность, от которых его не удалось спасти. На вскрытии недостаточности швов анастомоза не обнаружено.
Наконец, отдельные авторы (В. В. Виноградов) допускают, что при диффузном хроническом панкреатите рациональной операцией может быть панкреато-дуоденальная резекция. Общеизвестна техническая трудность и огромная травматичность этой операции, дающей высокий процент послеоперационной смертности. Даже при раке поджелудочной железы целесообразность такой операции сомнительна, так как больные, которым наложен обходной Пилиодигестивный анастомоз, живут в среднем столько же, сколько больные после радикальных операций (Е. С. Футорлн). Большой риск этого вмешательства для жизни Гшльного при хроническом панкреатите не может считаться оправданным.
Операции на внепеченочных желчных путях
Операции на билиарном тракте в силу близких анатомических и функциональных взаимоотношений желчных путей и поджелудочной железы издавна выполнялись при разнообразных заболеваниях последней.
Больше половины больных хроническим панкреатитом имеют те или иные патологические изменения желчных протоков — камни, стриктуры, папиллит, дискинезии, опухоли, варианты или аномалии анатомического строения.
Не случайно поэтому удельный вес оперативных вмешательств на внепеченочных желчных протоках и желчном пузыре при хроническом панкреатите всегда был и остается высоким. Это, в частности, показал в своей монографии И. Г. Руфанов еще в 1925 г.
Среди различных причин повторных операций так называемого постхолецистэктомического синдрома довольно часто встречаются своевременно не распознанный или вновь развившийся хронический панкреатит и его осложнения. Так, из 297 больных, детально обследованных в институте по поводу жалоб, возникших у них в разные сроки после холецистэктомии, у 93 они были обусловлены хроническим рецидивирующим панкреатитом, у 15 — индуративным панкреатитом со сдавленней холедоха и у 11 — рубцовым стенозом фатерова соска. Таким образом, на долю хронического панкреатита и его осложнений приходится более 40%' всех больных с болевым синдромом после холецистэктомии.
В относительно ранней стадии холецистопанкреатита при выраженном воспалительном процессе в желчном пузыре или камнях в нем операцией выбора является холецистэктомии. Устранение первопричины заболевания, ликвидация источника тяжелых печеночных колик, удаление основного очага патологического процесса чрезвычайно благотворны и, главное, способствуют стиханию воспалительного процесса в поджелудочной железе.
У 140 наших больных операция была закончена холецистэктомией. Со стороны поджелудочной железы у них были обнаружены разнообразные изменения — от рубцово-спаечного перипроцесса до индуративного панкреатита, который, однако, развивался, не сдавливая холедоха. В главе III мы подробно разобрали особенности и степень развития воспалительно-дегенеративных изменений в поджелудочной железе при хроническом холецистопанкреатите, рецидивирующем и индуративном панкреатите. У ряда этих больных холецистэктомии была не только санацией, поскольку воспалительный процесс в 2/з случаев начинался с желчного пузыря, но приводила к полному выздоровлению.
Больная Б. 51 года, страдала болями в животе, метеоризмом, неустойчивым стулом на протяжении 6 лет. Данные комплексного обследования позволили диагностировать хронический холецистопанкреатит. На операции обнаружено множество камней в желчном пузыре, перихолецистит. При телехолангиоскопии выявлен стойкий панкреатический рефлюкс, протоки нормальной ширины, головка поджелудочной железы уплотнена. Произведена холецистэктомия. После операции боли стали редкими и значительно менее интенсивными, а потом прекратились вовсе. Через 2 года больная практически не предъявляет жалоб, трудоспособна.
Данное наблюдение свидетельствует о стихании воспалительного процесса в поджелудочной железе после ликвидации основного механизма в системном заболевании.
Рецидивирующий калькулезный холецистопанкреатит служит показанием к операции даже в тех случаях, когда
OB сопровождается признаками недостаточности сфинктера Одди.
Больная Ш. 46 лет, страдающая приступообразными болями н эпигастрии и в левом подреберье около 5 лет, за последние годы стала отмечать опоясывающие боли в животе, головные боли, приступы острой слабости вплоть до коллапса. Год назад у нее был удален левый надпочечник по подозрению на опухоль, причем было отмечено уплотнение хвоста поджелудочной железы. Во время повторной операции в области шейки желчного пузыря найден одиночный камень, при измерении давления в холедохе диагностирована гипотония протоков (70 мм вод. ст.). Произведена холецистэктомия. После операции больная отметила значительное улучшение состояния, однако неоднократно обращалась к нам и лечилась амбулаторно. Ее временами беспокоили несильные тянущие боли в правом подреберье, иногда озноб, особенно мосле приема большого количества пищи. Явления хронического холангита были связаны у нее с недостаточностью сфинктера Одди и постоянным инфицированием протоков ферментативно активной флорой двенадцатиперстной кишки.
Особенно тщательно следует взвешивать показания к холецистэктомии при бескаменных холецистопанкреатитах. Операция может быть выполнена только при уверенности в поражении желчного пузыря, ибо необоснованное удаление последнего может привести к значительному ухудшению состояния больного.
При этом необходимо помнить о существовании так называемых шеечных бескаменных холециститов, при которых в основе заболевания лежат морфологические изменения слизистой оболочки и подслизистого слоя шейки пузыря и пузырного протока с развитием в них пролиферативного воспаления. Косвенным, но наиболее объективным показателем подобных изменений является значительное нарушение пассажа контрастного вещества через суженный, извитой и деформированный пузырный проток. При таких изменениях пузырь уже не может адекватно выполнять присущие ему функции и должен быть удален как источник болевых приступов, развивающихся на фоне панкреатита или без него.
В связи с тем что диагноз «шеечного» холецистита достаточно ответствен, а при клинико-рентгенологическом исследовании удается получить лишь косвенные признаки заболевания, мы во всех случаях производили тщательное исследование желчного пузыря во время операции с помощью рентгеноманометрии.
Необходимо заметить, что в ряде случаев, по нашим данным, почти у 7з больных бескаменным холециститом,
наблюдаются сочетанные поражения. Наряду с изменениями в области шейки желчного пузыря имеют место поражения терминального отдела общего желчного протока и фатерова соска (рубцовый папиллит, стриктуры). Совершенно очевидно, что успех операции будет полностью зависеть от адекватной коррекции всех имеющихся изменений.
Поэтому при наличии «шеечного» холецистита необходимо особенно тщательное исследование во время операции и гепатикохоледоха. При этом мы особое значение придаем телехолангиоскопии и зондированию фатерова соска эластическими пластмассовыми зондами.
При выявлении сочетанных поражений в желчном пузыре и желчевыводящих протоках необходимо, помимо холецистэктомии, производить и сфинктеротомию или наложить билиодигестивный анастомоз.
Огромная роль холедохолитиаза в патогенезе хронического панкреатита была показана в работах многих отечественных и зарубежных авторов. В самом деле, желчные камни в общем желчном протоке, у устья вирсунгова протока неизбежно должны провоцировать болевые приступы вследствие обтурации холедоха и активирования протеолитических ферментов в поджелудочной железе. Длительно протекающий холедохолитиаз нередко способствует грубой деформации протоков, которая может привести к образованию стриктуры. Поэтому во время операции по поводу хронического панкреатита особое внимание следует уделять всестороннему исследованию гепатикохоледоха. Речь идет о телехолангиоскопии, холангиографии, зондировании правого и левого печеночных протоков и дистальной части холедоха, пальцевом и визуальном обследовании его стенок, головки поджелудочной железы и близлежащих органов.
Показанием к холедохотомии являются конкременты, стриктура гапатикохоледоха или признаки обтурации дистальной части общего желчного протока и фатерова соска (рубцовый стеноз, камень, опухоль). После вскрытия холедоха в неясных случаях целесообразно прибегать к холедоскопии. Для этой цели лучше использовать гибкий фиброхоледохоскоп, не имеющий отрицательных качеств жесткого металлического холедохоскопа.
После устранения первопричины заболевания (удаление конкрементов, замазки, ликвидация стриктуры) должен быть решен немаловажный вопрос о методе завершения холедохотомии. От этого нередко зависит успех всей операции. В большинстве случаев при этом используют наружное или внутреннее дренирование, глухой шов холедоха применяют реже.
Среди способов наружного отведения желчи в нашей стране большое распространение получил Г-образный дренаж по А. В. Вишневскому. При всех его положительных качествах (обеспечивает декомпрессию желчных путей, не препятствует поступлению желчи в двенадцатиперстную кишку, легко удалим) он не лишен недостатков: существует возможность самостоятельного смещения и даже полного выхождения из протока, что может привести к желчному перитониту (мы наблюдали подобные осложнения у 4 больных, причем у 1 оно закончилось летально). В связи с этим при необходимости дренировать желчные протоки целесообразнее использовать расщепленный Т-образный дренаж (рис. 42).
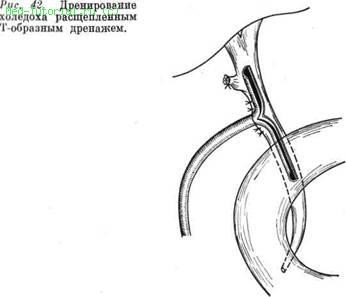
Он прочно удерживается в просвете холедоха даже без дополнительной фиксации его к стенкам протока, препятствует подтеканию желчи вокруг трубки и в отличие от дренажа Кера не травмирует общего желчного протока при извлечении.
Предложение Д. Л. Пиковского (1964) использовать для транспапиллярного дренирования протоков расщепленный дренаж не лишено основания. Этот дренаж представляет собой частично разрезанную вдоль резиновую трубку. Один из рассеченных концов низводится из общего желчного протока в двенадцатиперстную кишку. Другой (укороченный) остается в просвете печеночно-желчного протока. Нерассеченную стволовую часть дренажа выводят наружу. При этом способе дренирования создается свободный ток желчи как наружу, так и в просвет кишки и уменьшается опасность окклюзии вирсунгова протока. Мы считаем его небезопасным и не применяем.
Различные методы наружного дренирования желчных протоков не должны конкурировать между собой, ибо каждый из них имеет свои показания в связи с условиями каждого конкретного случая. Дренаж удаляют на 12—14-й день после операции. Перед этим производят его «тренировку». С этой целью на 7—9-й день дренаж начинают пережимать на несколько часов либо флакон для собирания желчи поднимают выше (ставят на тумбочку возле кровати, подвязывают к специальной стойке). Перед удалением дренажа мы, как правило, проводим фистулографию. Дренаж удаляем, убедившись в нормальном пассаже желчи в двенадцатиперстную кишку.
В отдельных случаях может быть использовано наружное чреспеченочное дренирование (рис. 43), особенно при оставлении дренажа в протоках на несколько месяцев.
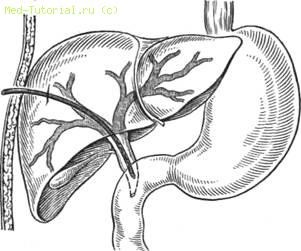
Рис. 43. Наружное чреспеченочное дренирование холедоха.
Ушивание раны холедоха наглухо встречает теперь меньше возражений, однако ограничений к его применению остается еще много и практически большинство хирургов используют его в относительно легких случаях: после удаления одиночного свободнолежащего камня, при диагностической холедохотомии и пр. Мы считаем возможным накладывать его и в осложненных случаях (мутная желчь, явления холангита, после зондирования фатерова соска и пр.), но одновременно дренируем просвет холедоха тонкой трубкой через пузырный проток. Это препятствует развитию желчной гипертензии, чреватой опасным просачиванием желчи между наложенными швами. Для лучшей герметичности используем непрерывный шов и покрываем его поверхность циакриловым клеем.
Ряд недостатков наружного дренирования гепатикохоледоха: длительная потеря желчи и вынужденное положение больного в постели (неблагоприятные в послеоперационном периоде), травма стенки протока при удалении дренажа, образование рубцовой стриктуры в месте дренирования заставили в ряде случаев предпочитать внутреннее дренирование желчных протоков. С этой целью используют различные билиодигестивные анастомозы, чаще холедоходуодено- и холедохоеюностомию.
Постоянное внутреннее дренирование особенно целесообразно при отсутствии уверенности в полном удалении мелких камней или замазки, подозрении на наличие конкрементов во внутрипеченочных протоках и пр. Мы считаем, что к нему следует прибегать также и при значительном расширении диаметра гепатикохоледоха (12—16 мм). Анастомоз в этих случаях способствует адекватному оттоку желчи и обеспечивает отхождение в кишечник оставленных или вновь образованных конкрементов при застое желчи в расширенных протоках.
Анастомоз мы накладываем однорядными узловыми швами синтетической нитью на атравматической игле. В подавляющем большинстве случаев используем двенадцатиперстную кишку, однако при выраженном дуоденостазе, нередко сопровождающем хронический панкреатит, а также при вовлечении кишки в патологический процесс, например при злокачественных опухолях фатерова соска или головки поджелудочной железы, используем для анастомоза сегмент тощей кишки, выключенной по методу Ру или с помощью энтероэнтероанастомоза.
Опыт этих операций у более 350 наших больных с различными изменениями гепатикохоледоха и фатерова соска, а также при хроническом панкреатите, основанный на изучении отдаленных результатов, свидетельствует о большой целесообразности подобных вмешательств. Опасность забрасывания в желчные протоки кишечного содержимого, якобы способствующего развитию хронического холангита, следует считать преувеличенной.
Вместе с тем при наложении билиодигестивного анастомоза по поводу хронического панкреатита следует помнить о некоторых особенностях, недооценка которых может свести на нет усилия хирурга и незаслуженно дискредитировать операцию.
Во-первых, гидравлическое давление в желудке всегда заведомо выше давления желчи в протоках, поэтому любой анастомоз с желудком обречен на неудачу. Во-вторых, необходимо объективно оценить моторно-эвакуаторную функцию того отрезка желудочно-кишечного тракта, с которым будет наложен анастомоз. При скрытом или явном дуоденостазе давление в двенадцатиперстной кишке нередко превышает давление желчи в протоках, поэтому анастомоз будет функционировать как бы в обратном направлении, и больные через некоторое время снова вернутся в клинику с симптомами холангита и мучительным болевым синдромом. Чтобы избежать этого, необходимо тщательно изучить функцию двенадцатиперстной кишки перед операцией и в случае подозрения на скрытый или явный дуоденостаз не накладывать анастомоза с двенадцатиперстной кишкой.
В этих случаях идеальным органом для анастомоза с желчными протоками является тощая кишка. Правда, наложение дополнительного U-образного анастомоза по Ру или брауновского межкишечного соустья усложняет операцию и удлиняет время вмешательства. Кроме того, выполнить холедохоеюноастомоз при относительно узком холедохе технически также более сложно. Важно также избрать оптимальный размер анастомоза (около 2—3 см), так как узкий анастомоз может зарубцеваться и способствовать нежелательной задержке кишечного содержимого в протоках.
Таким образом, суцрадуоденальная холедоходуоденостомия является наиболее рациональным и технически
простым вариантом соустья между общим желчным пророком и двенадцатиперстной кишкой при условии ее полноценной моторно-эвакуаторной функции (рис. 44).
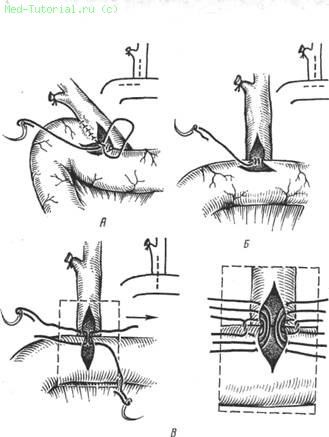
Рис. 44. Холедоходуоденоанастомоз. А — по Финстереру; Б — по Флеркену; В — по Юрашу.
Показаниями к сунрадуоденальнои холедоходуоденостомии служат обтурирующие формы индуративного панкреатита, протяженные рубцовые стриктуры терминального отдела холедоха и стенозы фатерова соска, когда устранение последнего не представлялось возможным.
Больной В. 69 лет, считавшей себя больной 14 лет, в 1963 г. произведена холецистэктомия. Зимой 1968 г. появилась желтуха. Па операции обнаружено, что поджелудочная железа плотная, бугристая, имеет вид опухоли, сдавливающей желчные пути. Произведена холедохотомия и дуоденотомия. Однако пройти через фа теров канал не удавалось даже тонким зондом. Наложен холедоходуоденоанастомоа. Медленное выздоровление.
В отдельных случаях для отведения желчи может быть использован и желчный пузырь, который обычно анастомозируют с изолированной петлей тощей кишки. Эта операция, однако, возможна лишь при отсутствии воспалительных изменений стенки желчного пузыря, конкрементов в нем и хорошей проходимости пузырного протока. Поскольку эти условия при хроническом панкреатите встречаются редко, это вмешательство не нашло широкого применения. Кроме того, путь поступления желчи в кишечник в этом случае более сложный, что играет отрицательную роль для полного восстановления функции желчеотделения и пассажа панкреатического сока.
В главе о патогенезе хронического панкреатита мы уже показали, что при этом заболевании у больных часто бывают дуоденит и скрытые функциональные формы дуоденостаза, проявляющиеся при дуоденокинезиографии гипокинетическим типом моторики кишки.
С другой стороны, при хроническом панкреатите вследствие длительных болевых кризов развивается тяжелый невроз, перераздражение нервных ганглиев, заложенных в кишечной стенке, серией патологических импульсов, поступающих из зоны раздраженной поджелудочной железы и солнечного сплетения.
А. П. Мирзаев и М. А. Петушинов (1967, 1968), изучив интрамуральный нервный аппарат стенки двенадцатиперстной кишки у больных хроническим панкреатитом, обнаружили в структуре нервных окончаний кишечной стенки грубые дистрофические изменения с появлением «клеток раздражения», вакуолизацией нейронов и распадом нервных клеток.
В настоящее время подавляющее большинство авторов считают, что достаточно широкое соустье между холедохом и двенадцатиперстной кишкой, обеспечивающее адекватное дренирование желчных путей, страхует от возникновения холангита и служит залогом выздоровления больных. В литературе обсуждаются в основном вопросы техники наложения холедоходуоденоанастомозов, в то время как функциональным особенностям последнего, особенно в отдаленном периоде, отводится незаслуженно мало места. Однако в последних работах (Б. В. Петровский, 1969; Е. В. Смирнов, 1969; С. В. Рынейский и Ю. А. Морозов, 1969; В. И. Соколов, 1968, 1969; Т. В. Шаак, 1967, и др.) авторы вновь обращают особое внимание на расстройство моторики двенадцатиперстной кишки при панкреатитах. Будучи вовремя не распознанным, оно, как мы сможем убедиться ниже, является причиной неудовлетворительной функции холедоходуоденоанастомоза, основой упорных холангитов и рецидивирующих панкреатитов.
Трансдуоденальная папилло- и сфинктеротомия самостоятельно применяются обычно при камнях, ущемленных в фатеровом соске, а также при резких рубцовых стенозах последнего. Большинство хирургов сочетают их с супрадуоденальной холедохотомией, которую используют для проведения зонда, облегчающего обнаружение фатерова соска и рассечение последнего.
После мобилизации двенадцатиперстной кишки по Кохеру фатеров сосок выпячивают с помощью зонда вместе с задней стенкой двенадцатиперстной кишки. Над этим участком производят небольшую дуоденотомию и по зонду скальпелем рассекают рубцово-измененную часть сфинктера Одди (рис. 45).
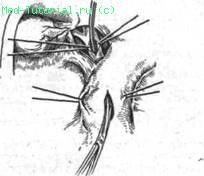
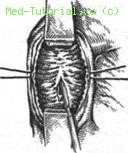
Рис. 45. Этапы трансдуоденальной папиллотомии.
Для удобства дозированного рассечения фатерова соска предложены различные зонды с оливой, имеющей специальный желобок, благодаря чему выполнение данной манипуляции наиболее безопасно. При необходимости на слизистую оболочку стенки двенадцатиперстной кишки и протока накладывают несколько узловых швов.
Операцию заканчивают ушиванием отверстия двенадцатиперстной кишки и наружным дренированием холедоха. От транспапиллярного дренажа в настоящее время большинство хирургов отказались в связи с развитием в
послеоперационном периоде тяжелых обострений панкреатита и даже панкреонекроза. Мы потеряли одну больную из-за такого осложнения.
Больная Ш. 17 лет, была оперирована в сельской больнице в Якутии. В клинику поступила с диагнозом: наружный желчный свищ, состояние после холецистэктомии. При повторной операции выяснилось, что не был диагностирован рубцовый стеноз фатерова соска на почве папиллита, вызвавший стойкую механическую желтуху и билиарный цирроз печени. Была выполнена дуоденотомия, холедохотомия и папиллотомия с оставлением транспапиллярного дренажа.
Послеоперационный период протекал очень тяжело. У больной развился послеоперационный панкреатит, вызвавший расхождение швов двенадцатиперстной кишки и перитонит. Смерть наступила через 16 дней после операции.
При сочетании резкого стеноза фатерова соска, осложненного часто рецидивирующим панкреатитом, со значительным расширением гепатикохоледоха или холедохолитиазом, мы с успехом иснользуем двойное дренирование общего желчного протока путем одновременного наложения холедоходуоанастомоза и сфйнктеротомии.
При начальных стадиях стеноза фатерова соска ряд авторов (Н. И. Махов и др.) рекомендуют бужирование его эластическими бужами. Помимо опасности этой манипуляции (образование ложного хода, повреждение ткани поджелудочной железы или задней стенки двенадцатиперстной кишки), очень сомнительна и результативность данного метода, поскольку рецидив рано или поздно неизбежен. Несмотря на ряд положительных сторон операции папиллосфинктеротомии — создание наиболее короткого пути оттока желчи и панкреатического сока в кишечник, возможность ревизии фатерова соска и коррекция обнаруженных изменений, она таит в себе ряд опасностей и осложнений. К ним относятся повреждения стенки двенадцатиперстной кишки и поджелудочной железы в связи с попытками создания более широкого соустья, чреватые развитием панкреонекроза, забрюшинных флегмон, перитонита и дуоденальных свищей.
Даже у сторонников данной операции летальность колеблется в пределах 6—7,3% (А. В. Смирнов с соавт. Wolf е. а.). На повышенный риск данного вмешательства указывают Е. В. Смирнов и В. С. Можайский, П. Н. Напалков и Н. А. Пострелов, К. Д. Тоскин и др.
После папиллотомии, а также иногда, когда из-за технических трудностей не удается выполнить адекватное
рассечение фатерова соска, нередко возникают рецидивы. По данным Wolf с соавт. в 20 %' случаев потребовалась повторная сфинктеротомия.
На специальном симпозиуме, проходившем в 1970 г. в Москве, в НИИ клинической и экспериментальной хирургии Министерства здравоохранения СССР, было высказано общее мнение о том, что показаниями к операциям папилло- и сфинктеротомии служат выраженные изолированные стриктуры и вколоченные камни фатерова соска. В осложненных случаях следует предпочесть обходные билиоди. Поэтому хирургическая коррекция этого состояния издавна была предметом споров.
По современным представлениям, среди причин различных нарушений пассажа содержимого двенадцатиперстной кишки наиболее часто встречаются функциональные дуоденостазы. Так, по данным М. Ф. Выржиковскои, только в 1 5% дуоденостаз возникает вследствие органического стеноза и в 98,5% случаев он является функциональным. Большинство отечественных авторов объясняют природу функциональных дуоденостазов нервнорефлекторным механизмом, имеющим место при различных нарушениях органов брюшной полости и в первую очередь панкреатодуоденальной зоны. Напалков, длительно занимавшийся проблемой дуоденостаза, разделяет их на первичные, самостоятельные и вторичные, возникшие как следствие основного заболевания. Последние требуют прежде всего лечения первичного заболевания и лишь при особых показаниях нуждаются в дополнительных хирургических вмешательствах, направленных на ликвидацию сопутствующих явлении дуоденостаза. Первичные, самостоятельные дуоденостазы могут потребовать различных операции: разделения сращений, вызывающих перегибы кишки, дуоденоеюноанастомозов разных вариантов, резекции желудка и т. п. По этому поводу П. Н. Напалков пишет: «Каждая из этих операций выполненная при обоснованных показаниях, дает, по нашему опыту, успех; выполненная без должного анализа заболевания, она может дискредитировать попытку хирурга помочь больному».
Среди операций, которые призваны устранить застои в двенадцатиперстной кишке, разгрузить кишку и тем самым устранить дуоденальный стаз, следует назвать резекцию желудка. Малоподвижная, значительно расширенная двенадцатиперстная кишка при этой операции выключается и желудочное содержимое переходит непосредственно в тощую кишку, что создает условия для лучшего пищеварения Смирнов, В. И. Петров, Bartlet и Nardi полагают, что резекция желудка, кроме того, способствует секреции поджелудочной железы в результате пересечения ветвей блуждающих нервов. Это оказывает также положительное влияние при болевых панкреатитах.
Вместе с тем значение резекции желудка при хроническом панкреатите многие авторы оспаривают (Sarlies, Mercadier) в связи с рецидивом болевых приступов. Мы также считаем, что к этой операции следует прибегать лишь при сочетанном поражении, например, желудка (язвенная болезнь) и поджелудочной железы (хронический рецидивирующий панкреатит). Вместе с тем при выраженном дуоденальном стазе с приступами болевого панкреатита резекция желудка оказывается благом. В отдельных случаях резекцию желудка целесообразно сочетать с постганглионарной невротомией.
Демонстративен следующий пример.
Больная Л. 60 лет, страдала холециститом с частыми обострениями. В 1941 г. ей произведено удаление желчного пузыря, заполненного гнойной желчью и камнями. С 1946 г. больную настойчиво лечат от гепатита, гастрита, панкреатита; за последние годы она лежала в хирургических клиниках 5 раз. С 1965 г. отмечает почти постоянные опоясывающие боли в верхней части живота, отрыжку, рвоту, мучительное чувство тяжести в животе. При обследовании диагностирован хронический панкреатит, дуоденостаз.
На операции двенадцатиперстная кишка мобильна, расширена, имеется выраженный рубцовый перидуоденит. Поджелудочная железа уплотнена, между ней и задней стенкой желудка — массивный рубцовый перипроцесс. Дуоденотомия; пуговчатый зонд свободно введен в холедох через зияющий фатеров сосок, диагностирована недостаточность сфинктера Одди. Произведена резекция желудка по Финстереру. Больная выздоровела.
Оставленный без внимания дуоденостаз может повлечь тяжелые осложнения, особенно когда принимают решение делать резекцию желудка по способу Бильрот I или когда создают внутренний дренаж желчных путей. При дуоденостазе анастомоз с двенадцатиперстной кишкой не может привести к успеху.
При язвенной болезни, осложненной хроническим панкреатитом, резекция желудка способствует ликвидации причины заболевания и потому действует благотворно, способствуя стиханию воспалительного процесса в поджелудочной железе.
Операции на нервной системе
У значительной группы больных, часть из которых перенесли неоднократные операции по поводу хронического панкреатита, иногда единственным методом лечения для снятия жестокого болевого синдрома является денервация поджелудочной железы.
Первую операцию такого рода произвел в 1940 г. Leriche, который выполнил местную анестезию нервных веточек в бассейне чревной артерии. Wertheimer в это же время произвел правостороннюю спланхникэктомию при раке поджелудочной железы. Наиболее полно теоретически обосновал целесообразность выполнения операции на вегетативной нервной системе Mallet-Guy в 1942 г. В том же году он произвел левостороннюю спланхникэктомию больному, у которого дренаж желчной системы не давал успеха. К 1945 г. он уже опубликовал результаты 10 операций такого рода с благоприятным исходом, к 1956 г. подобное вмешательство он выполнил более чем у 60 больных.
При хроническом панкреатите, развившемся в связи с гипотонией сфинктера Одди, Mallet-Guy предложил в качестве специального приема правостороннюю спланхникэктомию, основываясь на том, что правый чревный нерв уменьшает тонус сфинктера Одди. При гипертонии сфинктера Одди он рекомендовал комбинировать сфинктеротомию с дренажом протока и ваготомией, поскольку вагус усиливает тонус сфинктера.
Механизм иннервации сфинктера Одди и тонкая структура функционирования папиллы при разнообразных патологических состояниях желчных путей и фатерова соска все еще мало изучены, поэтому весьма трудно правильно оценить патогенетическую целесообразность и рациональность этих операций.
Однако к 1965 г. Mallet-Guy собрал наблюдения уже о 207 спланхникэктомиях в сочетании с левосторонней ганглиоэктомией. Выздоровление наблюдалось в 85% случаев, улучшение — в 7,8%. Было получено 7 летальных исходов, ухудшение в 7,2% случаев. У алкоголиков, страдающих хроническим болевым панкреатитом, хорошие результаты после этой операции Mallet-Guy отмечает только в 75%.
Экспериментальные данные и значительный клинический материал позволили автору рассматривать операции на нервной системе не как паллиативные, имеющие целью лишь прерывание рефлекторного нервного пути, но и как причинные, патогенетические, снимающие хроническое раздражение нервных окончаний, нормализующие трофику органа и приостанавливающие развитие патологического процесса в железе. Эти операции, подавляя болевой синдром, субъективно улучшают состояние больных, прибавляющих после этого массу тела на 10—18 кг, способствуют нормализации объективных показателей, предупреждают образование новых очагов дегенерации и склероза ткани поджелудочной железы.
Вслед за Mallet-Guy операции на вегетативной нервной системе стали выполнять многие зарубежные хирурги. Так, Grimson, Hasser и Hitchin (1947) разработали методику удаления чревных ганглиев и полной резекции солнечного сплетения. Rienhofr и Backer (1947) предложили двустороннюю ваготомию в сочетании с радикальной симпатэктомией и одновременной двусторонней резекцией большого и малого чревных нервов.
Tokats и Walter (1947) для лечения хронического панкреатита резецировали чревные нервы либо удаляли всю паравертебральную симпатическую цепочку — от IX до XII узла. В дальнейшем при хроническом панкреатите авторы предлагали широко применять лечебно-диагностические паравертебральные блокады, и, если эффект был недостаточным или кратковременным, производить пересечение чревных нервов с обеих сторон либо сочетать одностороннюю невротомию с нижней дорсальной симпатэктомией.
Японские хирурги Ioschioka и Wakabayachi (1950) предложили для лечения хронического болевого панкреатита производить постганглионарную невротомию. Суть метода состоит в пересечении нервных стволиков, идущих от узлов солнечного сплетения к головке и телу поджелудочной железы. Кроме устранения наиболее тягостного симптома — постоянных изнуряющих болей, невротомия по Ioschioka и Wakabayachi создает относительный покой для больного органа, снижает восприимчивость к патологическим раздражителям, улучшает кровообращение и способствует нормализации секреторного процесса.
В 1951 г. французский хирург Latarijet произвел с хорошим клиническим результатом пересечение нервных веточек вокруг печеночной артерии в сочетании с холецистодуоденостомией. Позднее Placac и Vorreith (1960) повторили эту операцию, но с меньшим терапевтическим эффектом.
В нашей стране операции на вегетативной нервной системе при лечении хронического панкреатита применяются около 10 лет. Наибольшее распространение получили симпатэктомии (Б. А. Петров и Ф. X. Новрузов, 1967), постганглионарные невротомии по Ioschioka, Wakabayachi (В. Ш. Работников, I960; А. В. Смирнов и Л. П. Волкова, 1964; Е. В. Смирнов и О. Б. Порембский, 1965; М. А. Трунин, 1965), маргинальные невротомии поджелудочной железы (П. Н. Напалков, М. А. Трунин и И. Ф. Крутикова, 1967; М. А. Трунин, 1965, 1967, 1968), селективные невротомии ветвей чревной артерии.
При диффузных панкреатитах с различной локализацией участков фиброза М. А. Трунин производит операцию, которая состоит в пересечении нервных волокон, расположенных по периметру поджелудочной железы. Эта операция, так называемая маргинальная невротомия, менее травматична, чем операция по Ioschioka и Wakabayachi, поскольку не требует полной мобилизации двенадцатиперстной кишки и головки поджелудочной железы.
Маргинальная невротомия дает удовлетворительные и хорошие результаты не только в случаях изолированного заболевания головки, но и при тотальном поражении поджелудочной железы, так как при ней перерезают симпатические и парасимпатические нервные волокна, что снимает боль, уменьшает секрецию железы и предотвращает рецидив заболевания.
Операции такого рода были выполнены нами либо в -самостоятельном виде, либо как дополнение к основному оперативному вмешательству, чаще на желчных путях или желудке. У всех больных ведущим клиническим признаком заболевания были боли, постоянные или периодические, короткие или длительные, более или менее выраженные, но всегда мучительные, изнуряющие, доводящие до наркомании и тяжелой инвалидности.
У всех больных выраженность симптоматики и жестокий болевой синдром заставили предпринять оперативное вмешательство. В начале нашей работы производили пересечение нервных ветвей между чревными ганглиями и поджелудочной железой, а при так называемом головчатом панкреатите прибегали к постганглионарнои невротомии по Ioschioka и Wakabayachi. В дальнейшем мы считали более оправданной маргинальную невротомию, когда пересекают нервные веточки по периметру поджелудочной железы, как по верхнему, так и по нижнему краю.
Технически это вмешательство выполняется следующим образом. После лапаротомии срединным разрезом через Lig. gastrocoHcum обнажают поджелудочную железу, над которой по верхнему краю рассекают брюшину. В отдельных случаях доступ целесообразнее осуществлять через малый сальник. Определяют ствол и ветви чревной артерии, справа и слева от которой лежат чревные узлы нервного сплетения. После подведения под них раствора новокаина со спиртом (до 20 мл с каждой стороны) пересекают нервные веточки вокруг ствола чревной артерии и нервные стволики вдоль и вокруг печеночной и селезеночной артерий. Последнюю, расположенную по верхнему краю поджелудочной железы, следует освобождать на всем протяжении — от головки до хвоста. Операцию заканчивают пересечением нервных веточек по нижнему краю поджелудочной железы, в бассейне верхней брыжеечной артерии (рис. 46).
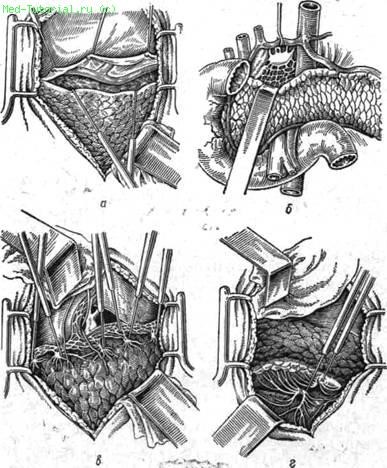
Рис. 46. Этапы операции невротомии поджелудочной железы. о — рассечение капсулы; б — обнажение правого чревного узла- в — невротомия по верхнему краю железы; г —невротомия по нижнему краю
У всех больных, перенесших эту операцию, в клинике заболевания преобладал болевой синдром. На операции были найдены диффузные изменения в поджелудочной железе по типу опухолеподобной дегенерации или грубый рубцово-спаечный перипроцесс. На рис. 47 схематично представлены утолщенные нервные веточки вокруг ствола чревной артерии, имеющиеся, как правило, у больных в поздней стадии хронического панкреатита.
Приведем следующее наблюдение.
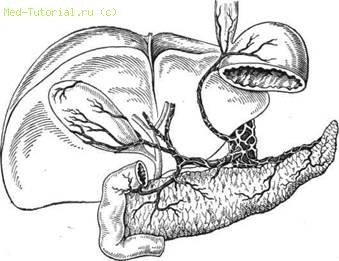
Рис. 47. Гипертрофия нервных ветвей в бассейне чревной артерии при хроническом панкреатите.
Больной Н. 39 лет, в 1968 г. удален желчный пузырь в связи с хроническим холецистопанкреатитом. В октябре 1969 г. поступила в наш институт по поводу постоянных болей в эпигастрии, тошноты, рвоты во время приступа, резкого похудания, отмечалась тяжелая депрессия. Больная имеет инвалидность I группы. Скеннирование выявило резкое снижение накопления радиоактивного селенметионина в панкреатической ткани; углеводная кривая беспрофильная, плоская; в кале — стеаторея, креаторея. Во время операции обнаружен грубый склеротический процесс в ткани поджелудочной железы, выраженный спаечный перипанкреатит. Произведена полная маргинальная невротомия поджелудочной железы. Спустя год больная чувствует себя хорошо, работает, увеличилась масса тела, боли беспокоят редко.
Наблюдения за оперированными больными показали, что хорошие отдаленные результаты были отмечены в тех случаях, когда маргинальная невротомия была проведена в более ранние сроки заболевания.
Так, у больной Ф. 34 лет, страдающей хроническим панкреатитом 5 лет, на операции было обнаружено, что поджелудочная железа плотная в области тела и хвоста, имеются сращения между железой и желудком. При холецистохолангиографии — затрудненное опорожнение желчного пузыря, получен стойкий панкреатический рефлюкс, гепатикохоледох не расширен. Произведены холецистэктомия и маргинальная невротомия больше по ходу селезеночной артерии, учитывая преимущественно левостороннюю локализацию воспалительного процесса в поджелудочной железе. Боли ликвидированы. Больная выздоровела.
Некоторые отечественные хирурги при хронических панкреатитах производят частичную десимпатизацию печеночной (В. В. Виноградов, 1966) или селезеночной (М. А. Трунин, 1968) артерий. По мнению Б. А. Петрова, целесообразность этих операций сомнительна, так как эффект их неполный или кратковременный.
Мы, как правило, применяем маргинальную невротомию в полном объеме, мобилизуя печеночную и селезеночную артерию, приподнимая на резиновых держалках весь ствол чревной артерии и пересекая чревные веточки под ним. Вторым этапом производили невротомию в бассейне верхней брыжеечной артерии. Лишь в отдельных случаях мы ограничивались первым моментом операции, что было вызвано техническими трудностями.
Основными преимуществами операции маргинальной невротомии, по нашему мнению, являются следующие: малая травматичность, выключение из иннервации только поджелудочной железы и то, что эта операция может оказаться эффективной не только при изолированном поражении головки, но и при тотальном поражении поджелудочной железы.
В случаях локального поражения деструктивно-склеротическим процессом какой-то части поджелудочной железы возможна селективная невротомия в бассейне печеночной или селезеночной артерии (артериолиз) в сочетании с операцией, устраняющей непосредственную причину заболевания (холецистэктомия, холедохотомия, внутренний дренаж желчных путей, сфинктеротомия и т. п.). Изучив отдаленные результаты, мы пришли к заключению, что операция, выполненная в этом объеме, менее травматична, технически проще и достаточно эффективна.
Таким образом, операции на вегетативной нервной системе в лечении болевых форм хронического панкреатита без сомнения оправданы и должны предприниматься при соответствующих показаниях.
В послеоперационном периоде в первую очередь следует обращать внимание на реакцию со стороны поджелудочной железы, состояние желудочно-кишечного тракта и сердечно-сосудистой системы.
Наиболее опасными осложнениями считают послеоперационный панкреатит, парез кишечника, недостаточность швов наложенного билиодигестивного соустья, перитонит, диабетический криз, печеночно-почечная недостаточность, пневмония.
В связи с возможностью отека фатерова соска после операции или расстройства функции печени важен контроль за протромбиновым временем, уровнем билирубина, признаками желтухи.
Профилактически больному дают викасол, хлористый кальций, можно рекомендовать переливание крови.
Для компенсации функции печени вводят глютаминовую кислоту (по 10—20 мл 1%' раствора внутривенно в течение 5—10 дней), которая соединяется в тканях с аммиаком, образуя нетоксичный глютамин, способствующий выделению аммиака через почки в виде аммонийных солей, гемодез.
В результате пересечения нервных сплетений нередко наблюдается парез кишечника, который сопровождается икотой, рвотой, метеоризмом, задержкой стула и газов. В тяжелых случаях рвота становится упорной, происходит большая потеря жидкости и питательных веществ.
В этих случаях в течение 1—2 сут запрещается прием через рот жидкости и пищи. Питание дают на 2—3-й сутки после операции: бульон, творог, яйца, протертые супы, жидкая манная каша. Для борьбы с парезом внутривенно вводят 10 %! раствор хлористого натрия, производят двусторонние блокады по А. В. Вишневскому, назначают стрихнин. Хорошо восстанавливает перистальтику переливание крови. Большое значение имеет своевременное воет становление баланса электролитов, в частности калия.
Для ликвидации гипокалиемии внутривенно капельно (60 капель в минуту) вводят 1000 мл 5,%] раствора глюкозы, содержащий 6 г, т. е. 80 мэкв калия. Важно помнить, что быстрое введение калия в кровь может вызвать тяжелую реакцию вплоть до остановки сердца. Указанную дозу следует вводить в два приема с обязательным контролем содержания калия в крови.
Наиболее частым и тяжелым осложнением является острый послеоперационный панкреатит. Признаками панкреатита в послеоперационном периоде следует считать появление резких болей в подложечной области с локализованным напряжением мышц, ухудшение состояния, повышение температуры, лейкоцитоз, повышение уровня диастазы крови и мочи. Операционная травма, непосредственная травма поджелудочной железы, тяжесть состояния больных иногда Затрудняют распознавание этого раннего послеоперационного осложнения. Ведущим фактором в его развитии является остро наступившая непроходимость вирсунгова протока в результате реактивного отека поджелудочной железы.
Другой причиной можно назвать переход воспалительного процесса в верхнем этаже брюшной полости на поджелудочную железу. Такое развитие панкреатита наблюдалось в большей или меньшей степени у больных с язвенной болезнью желудка и двенадцатиперстной кишки, когда воспалительный процесс захватывал головку и тело поджелудочной железы, создавая благоприятную почву для острого воспаления поджелудочной железы.
Одной из причин послеоперационного панкреатита может явиться также скрытый или явный дуоденостаз.
После резекции желудка наиболее частой предпосылкой для дуоденостаза является перегиб приводящей петли кишки. При этом инфицированное содержимое двенадцатиперстной кишки проникает в выводные протоки поджелудочной железы, вызывая закупорку главного протока, застой панкреатического сока, отек, выход ферментов в межуточную ткань и аутолиз.
И. В. Старцев (1964), Luliani, Fulden (1956) и др. считают вероятным при дуоденостазе попадание в вирсунгов проток желчи, которая наряду с микроорганизмами раздражает поджелудочную железу и может явиться причиной ее воспаления.
Так, больному К. 56 лет, была произведена резекция желудка по поводу хронического панкреатита и дуоденостаза. Первые двое суток у больного были боли в эпигастрии, тошнота, срыгивание, рвота; затем начали прогрессировать явления перитонита, парез кишечника. На 9-й день после операции больной умер. На вскрытии было установлено, что двенадцатиперстная кишка предельно заполнена жидким содержимым, имеется некроз поджелудочной железы, прорезывание швов на культе кишки и перитонит.
Можно предположить, что в этом случае причиной панкреатита в условиях пареза и функциональной недостаточности сфинктера Одди было поступление инфицированного содержимого двенадцатиперстной кишки в главный панкреатический проток с последующим образованием реактивного, а затем некротического воспаления железы.
В некоторых случаях послеоперационный панкреатит был по сути рецидивом хронического процесса в железе. В этом смысле представляет интерес следующее наблюдение.
У больного П. 52 лет, страдавшего много лет язвенной болезнью желудка, хронический панкреатит как вторичное заболевание был диагностирован еще до операции. При лапаротомии была обнаружена пенетрация язвы в головку поджелудочной железы. С большим трудом удалось произвести резекцию желудка. Спустя двое суток после операции был диагностирован острый послеоперационный панкреатит, который мы расценили как обострение хронической формы заболевания. Диастаза мочи достигала 2048 ед. по Вольгемуту, лейкоцитоз возрос до 18-Ю3 в 1 мкл.
Благодаря комплексной терапии явления панкреатита удалось купировать. Больной выздоровел.
Диагностировать панкреатит, возникший после операций на органах брюшной полости, иногда бывает трудно.
Ведущими признаками могут быть нарастающие явления перитонита, характерные опоясывающие боли и ухудшение общего состояния больного в первые 2—3 дня после операции, а также развитие стойкого пареза кишечника.
В выраженных случаях отличительной особенностью клиники является интоксикация, нередко сопровождающаяся сосудистым коллапсом.
Различают так называемый ранний коллапс, возникший через 8—24 ч после операции, и поздний коллапс, развивающийся на 2—3-й день на фоне прогрессирующего перитонита с генерализованным сужением сосудов, олигурией, падением артериального давления и т. п.
В последнем случае панкреатит возникает, по-видимому, в результате тяжелой интоксикации и гипокалиемии, сопровождающей экссудацию плазмы в перипанкреатические ткани и брюшную полость.
В таких случаях больной впадает в состояние глубокой прострации. Нередко наблюдаются эйфория, мягкий частый пульс, падение артериального давления при нормальной температуре и сравнительно «спокойном» животе.
Мы специально проследили закономерности развития послеоперационных панкреатитов на основании анализа 1926 операций на желудке, поджелудочной железе и желчных путях, которые были выполнены в клинике за 10 лет.
Из числа всех операций поджелудочная железа была вовлечена в той или иной мере в воспалительный процесс в 432 случаях, послеоперационный панкреатит наблюдался у 53 больных. Из них явления сосудистого коллапса наблюдались у 26 больных при следующих операциях (табл. 6).
Таблица 6 Развитие коллапса при послеоперационном панкреатите
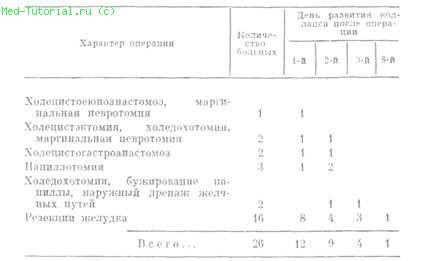
Как видно из табл. 6, ранний коллапс развился у 12 больных в первые 24 ч после операции, у остальных — на 2-е сутки (9 наблюдений), на 3-й сутки (4 наблюдения)", на 8-е сутки (1 наблюдение).
В лечении послеоперационных панкреатитов нужно применять комплексную терапию по определенной схеме. Во всех случаях, когда особенности операции позволяли предвидеть послеоперационный панкреатит, мы подводили к ложу железы тонкий полиэтиленовый катетер для орошения брюшной полости антибиотиками, а в тяжелых
случаях — для местного введения трасилола. Через этот же дренаж можно получить экссудат для определения в нем амилазы и других ферментов. Трасилол вводили внутривенно, капельно от 30 000 до 100 000 ед. 1—2 раза в сутки от 2 до 7 дней. Общее количество препарата в среднем 700 000—800000 ед. на курс лечения.
Большое значение придавали борьбе с болью, профилактике и раннему лечению тяжелого панкреатического шока (двусторонняя паранефральная новокаиновая блокада, внутривенное вливание 150—200 мл 0,25% раствора новокаина, эуфиллин, атропин с промедолом в чередовании с платифиллином и папаверином, нитроглицерин, сернокислая магнезия, местная гипотермия и т. п.).
Подавления активности сока поджелудочной железы и панкреатической секреции достигали назначением голодной диеты, аспирацией желудочного содержимого с помощью тонкого зонда, инъекциями 0,1% раствора сульфата атропина и т. п. Широко применяли переливание крови и белковых жидкостей, вводили сердечные и вазопрессоры (эфедрин, мезатон, норадреналин). Антибиотики назначали сразу после операции, используя препараты широкого спектра действия.
Десенсибилизация организма достигается обычно антигистаминными средствами (пипольфен, супрастин, димедрол, ветразин), в тяжелых случаях можно применить гидрокортизон (по 125—400 мг в сутки).
Большое значение следует придавать нормализации витаминного, водного и электролитного баланса (витамины А, С, группы В, калий, кальций, щелочные минеральные воды и т. п.). Показателями водно-солевого равновесия можно считать достаточный диурез (до 1500 мл) и стабильный уровень кальция в крови (до 10 мг).
Показания к релапаротомии при послеоперационных панкреатитах возникают при прогрессирующих явлениях перитонита. В случае деструктивного панкреатита следует дренировать полости малого сальника и желчевыводящую систему.
Таким образом, развитие острых панкреатитов после операции на желудке, двенадцатиперстной кишке, поджелудочной железе и внепеченочных желчных путях зависит от ряда причин, важнейшими из которых является переход воспалительного процесса на поджелудочную железу, острый послеоперационный дуоденостаз и возможность обострения хронического панкреатита. В клинике этого грозного осложнения на первый план выступают интоксикация, протекающая с явлениями коллапса, умеренные опоясывающие боли в эпигастрии, вздутие живота, рвота, повышение диастазы в моче, увеличение лейкоцитов в периферической крови, появление признаков перитонита и прогрессирующее ухудшение состояния больного.
Наиболее эффективным является комплексное лечение послеоперационного панкреатита, предусматривающее консервативную терапию (белковые жидкости, трасилол, но вокаиновая блокада, вазопрессоры, переливание крови, введение наркотиков, сердечных, голод, местная гипотермия, стероиды по показаниям и т. п.), и рациональная оперативная тактика (релапаротомия, дренирований, брюшной полости).
