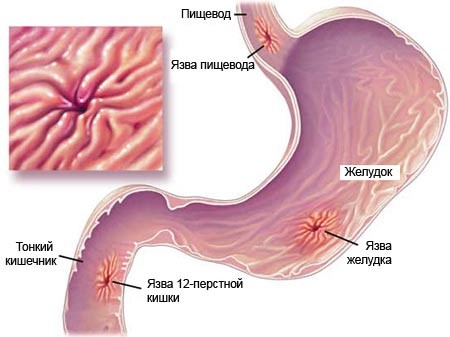
Эрозивное поражение желудка. или эрозивный гастрит относится к достаточно распространенным заболеваниям органов пищеварения. Эрозивные гастриты бывают острые и хронические.
Острый эрозивный гастрит — это поверхностное поражение слизистой оболочки желудка. Развивается он очень быстро, особенно провоцируемый различными стрессами.
Хронический эрозивный гастрит характеризуется множественными эрозиями слизистой оболочки желудка на разных стадиях заживления.
Среди множества заболеваний верхних отделов желудочно-кишечного тракта (ЖКТ) гастродуоденальные эрозии относятся к числу наиболее распространенных и наименее изученных.
Гастродуоденальные эрозии — это поверхностные дефекты слизистой оболочки желудка и двенадцатиперстной кишки, не выходящие за пределы ее собственной мышечной пластинки, которые образуются в очагах поверхностного некроза и заживают без образования соединительнотканного рубца.
Эрозии слизистой оболочки желудка и двенадцатиперстной кишки впервые были описаны итальянским анатомом Морганьи еще в 1761 году в труде «О месте нахождения и причинах болезней, выявленных анатомом», основанном на изучении обширного секционного материала. В последующем изучение процесса эрозирования слизистой оболочки гастродуоденальной зоны, главным образом как предъязвенного состояния, нашло отражение в трудах К. Рокитанского (1842).
По предложению K. Kawai и соавт. 30 лет назад стали различать острые (поверхностные, плоские) и хронические (полные, приподнятые, оспоподобные — вариолиформные) эрозии.
Острые эрозии — это поверхностные дефекты слизистой оболочки желудка, преимущественно его дистального отдела, диаметр которых не превышает 1–2 мм. Хронические эрозии — это возвышающиеся (приподнятые) участки слизистой оболочки желудка диаметром 3–7 мм, имеющие округлую форму, напоминают папулу с пуповидным вдавлением в центре, нередко с наличием на их вершине небольшого изъязвления («зрелые» полные эрозии).
Этиология и патогенез гастродуоденальных эрозий
Среди основных причин возникновения острых эрозий важную роль играют следующие:
1) прием лекарственных средств, включая нестероидные противовоспалительные препараты (НПВП), кортикостероиды, препараты дигиталиса, нитрофураны, толбутамид, верошпирон, этакриновую кислоту;
2) алкогольная интоксикация;
3) стрессовые воздействия (ожоги и обморожения, шок, ранения, политравма, психоэмоциональный стресс);
4) тяжелая соматическая патология (декомпенсированная недостаточность кровообращения, хроническая почечная и гепатоцеллюлярная недостаточность, заболевания крови, хронические неспецифические заболевания легких);
5) заболевания эндокринной системы (гиперпаратиреоз, сахарный диабет, сепсис).
По этиологии хронические эрозии подразделяют на первичные и вторичные. Первичные возникают, как правило, у практически здоровых молодых лиц без сопутствующих заболеваний под воздействием неблагоприятных социально-климатических или психотравмирующих факторов и способны подвергаться инволюции по мере устранения влияния последних.
Вторичные хронические эрозии возникают как эквивалент синдрома генерализованных циркуляторно-гипоксических расстройств, измененной иммунной реактивности и обменных процессов на фоне заболеваний сердечно-сосудистой системы и печени, ассоциированных с полными эрозиями с частотой до 75 %. По данным Л.И. Аруина, у 19,1 % больных эрозии протекают на фоне хронического гастрита, у остальных сочетаются с другими заболеваниями органов пищеварительной системы, в первую очередь с язвой двенадцатиперстной кишки (51 %) и хроническим холециститом (13 %).
Среди факторов, имеющих значение в развитии эрозий, изучается роль Helicobacter pylori (Нр), дуоденогастрального рефлюкса, соляной кислоты, снижения цитопротекторных свойств слизистого геля желудка, микроциркуляторных нарушений в слизистой оболочке желудка, иммунных нарушений, а также некоторых гормонов.
Факторы риска эрозирования слизистой оболочки желудка и двенадцатиперстной кишки
1. Нр-инфицирование. Согласно результатам современных исследований, контаминация слизистой оболочки Нр составляет 66–85 % при локализации эрозий в желудке. Некоторые авторы считают, что важная роль Нр в возникновении эрозий подтверждается не столько высоким уровнем контаминации слизистой оболочки желудка, сколько выраженным эффектом эррадикационной терапии, который четко коррелирует с частотой ликвидации эрозивных поражений.
2. Большинство исследователей важное значение придают нарушениям микроциркуляции в патогенезе эрозий слизистой оболочки желудка. При рецидивирующих эрозивных гастритах в фазе ремиссии нарушения локальной и общей микроциркуляции отмечаются в 62 и 40 % случаев соответственно по сравнению с 38 и 24 % у больных хроническим гастритом без эрозий, причем особенно выраженные изменения выявлены при изучении терминального кровотока.
3. Большое значение в формировании острых и хронических эрозий придают дуоденогастральному рефлюксу. По данным разных авторов, эрозии желудка сочетаются с последним в 22,9–85 % случаев. Компоненты дуоденального содержимого, прежде всего соли деконъюгированных желчных кислот и лизолецитин, в высоких концентрациях оказывают повреждающее действие на слизистую оболочку желудка.
4. Многие исследователи приводят данные о нарушениях моторной функции желудка и повышении внутриполостного давления. что вызывает вначале функциональное, а затем органическое поражение органа с формированием клинической картины заболевания. Так, в работе Е.В. Никишиной выявлена интрагастральная и интрадуоденальная гипертензия у 78 % больных эрозивным гастритом, а также отмечено преобладание гиперкинетического типа моторных нарушений желудка.
5. В некоторых случаях показано повышение в крови у больных с эрозиями содержания кортизола, гастрина, тиреотропного гормона и инсулина. С помощью корреляционного анализа авторы установили прямую зависимость между уровнем интрагастрального и интрадуоденального давления и содержанием гастрина, инсулина и тиреотропного гормона.
6. В последнее время появляется все больше работ, свидетельствующих о значении нарушений иммунитета в развитии хронических эрозий желудка.
7. Значение кислотно-пептического фактора в развитии хронических эрозий желудка однозначно не определено. И.В. Маев и соавт. (1998) сообщают о том, что хронические эрозии чаще встречаются на фоне высоких показателей желудочной секреции.
8. Особое место среди причин развития гастродуоденальных эрозий занимают нестероидные противовоспалительные препараты. Гастродуоденальные язвы возникают у 20–25 % больных, длительно принимающих указанные лекарственные средства, а эрозии слизистой оболочки желудка и двенадцатиперстной кишки — более чем у 50 % пациентов, при этом риск развития таких поражений сохраняется в течение нескольких месяцев после прекращения лечения.
Клиническая картина гастродуоденальных эрозий
Острые эрозии имеют четко очерченный клинический симптомокомплекс, на первый план выступают клинические признаки фоновых заболеваний. У 30–90 % лиц молодого возраста с неизмененной слизистой оболочкой острые эрозии могут протекать бессимптомно или клинические проявления достаточно скудны и неспецифичны. Чаще возникает изжога, отрыжка кислым, крайне редко — тощаковые и «голодные» боли в эпигастрии невысокой интенсивности. Для острых эрозий желудка характерно относительно частое (до 4,5 %) развитие геморрагических осложнений.
Для хронических эрозий проявления диспептического и болевого абдоминального синдромов достаточно выражены и специфичны. Отрыжка и изжога наблюдаются у 75 % больных с хроническими эрозиями, часто сочетаются с чувством тяжести в правом подреберье и метеоризмом. Периодические тощаковые и «голодные» боли в эпигастрии, наблюдающиеся у большинства больных с хроническими эрозиями, часто иррадиируют в позвоночник. Причем, если у больных молодого возраста преобладают ноющие и тупые боли, то в старшей возрастной группе боли на фоне нарастания чувства тяжести в эпигастрии носят преимущественно схваткообразный характер с развитием на их высоте тошноты, неустойчивого стула с преобладанием запоров.
Таким образом, в клинической картине хронических эрозий обнаруживается определенное сходство с симптомами дуоденальной локализации язвенного дефекта. Отмечено также достаточно частое формирование выраженных симптомов основных заболеваний. К ним относятся заболевания сердечно-сосудистой системы (артериальная гипертензия, ишемическая болезнь сердца) и печени (хронический гепатит и цирроз).
В то же время имеются работы, указывающие на неспецифичность клинической картины, которая складывается из болевых и диспептических синдромов различной степени выраженности. Я.С. Циммерман и соавт. также считают, что использовать клинические проявления с диагностической целью в отношении эрозивного гастрита невозможно.
Диагностика двух типов эрозий осуществляется с помощью фиброгастродуоденоскопического исследования. Однако полноценное суждение о характере эрозий можно составить лишь на основании гистологического исследования.
Развитию острых эрозий обычно предшествуют субэпителиальные геморрагии петехиального типа, но без нарушения целостности слизистой оболочки желудка, в связи с чем их нередко описывают как геморрагические эрозии. При гистологическом исследовании дефект слизистой оболочки желудка или двенадцатиперстной кишки, как правило, неглубокий, но занимает несколько валиков. Сроки эпителизации острых эрозий не превышают 2–7 дней.
Хронические эрозии располагаются в антральном отделе желудка в виде цепочек, идущих по направлению к привратнику, в количестве от 1 до 15. Глубина дефекта слизистой оболочки при хронических эрозиях почти такая же, как при остром эрозировании, их дно обычно образуют железы, реже — мышечная пластинка слизистой оболочки. Морфологически хронические эрозии характеризуются наличием коагуляционного некроза, который напоминает фибриноидный некроз при остром эрозировании, но без типичного для него фиброза краев. Гиперплазия пилорических желез в зоне хронической эрозии является причиной образования тех возвышений, которые служат эндоскопическим критерием. В области дна полных эрозий выявляется грануляционная ткань, а в краевых отделах — дистрофические и атрофические изменения эпителия желез.
Хронические эрозии существуют длительное время — от 4 недель до нескольких лет. Согласно мнению ряда авторов, данный тип эрозий по характеру гистологических изменений можно подразделить на «незрелые» и «зрелые». В первом случае эрозия проходит все стадии развития и эпителизируется, затем отек слизистой оболочки на месте ее выбухания остается постоянно в результате развивающегося фиброза тканей и выраженного продуктивного воспаления.
Лечение гастродуоденальных эрозий
Одной из наиболее важных и сложных проблем является лечение хронических эрозий желудка. Учитывая многогранность патогенеза, большинство авторов рекомендуют комплексное лечение эрозий с воздействием на различные звенья их патогенеза.
Терапия как острых, так и хронических эрозивных поражений желудка предполагает прежде всего устранение влияния неблагоприятных факторов экзогенного и эндогенного характера, то есть устранение стрессовых влияний, нормализацию режима и качества питания, отказ от курения и употребления алкоголя, приема препаратов с ульцерогенными свойствами.
Антисекреторные препараты предназначены для лечения гастродуоденальных эрозий, особенно протекающих с язвенноподобными проявлениями и выраженной гиперацидностью. Применяются ингибиторы протонной помпы (ИПП) — омепразол по 40 мг в сутки. Возможно применение блокаторов Н2-рецепторов (фамотидин по 40 мг в сутки в течение 4–6 недель с постепенной отменой).
Учитывая частое обнаружение в зоне эрозий Нр, рекомендуется лечение антихеликобактерными средствами в составе тройной или квадротерапии с использованием преимущественно де-нола, который не только способствует элиминации Нр, но и оказывает противовоспалительное и цитопротекторное действие.
Рекомендации II Маастрихтского консенсуса в качестве терапии первой линии включали следующие тройные схемы лечения: ИПП в стандартной дозе 2 раза в сутки (или ранитидин висмута цитрат) + кларитромицин по 500 мг 2 раза в сутки + амоксициллин по 1000 мг (или метронидазол по 500 мг) 2 раза в сутки на протяжении 7 дней.
В качестве терапии второй линии использовалась квадротерапия: ИПП в стандартной дозе 2 раза в сутки + висмута субцитрат по 120 мг 4 раза в сутки + тетрациклин по 500 мг 4 раза в сутки + метронидазол по 500 мг 3 раза в сутки.
ІІІ Маастрихтский консенсус внес следующие изменения в лечение хеликобактерной инфекции:
— терапия первой линии: ИПП + кларитромицин + амоксициллин (может использоваться метронидазол при первичной резистентности к кларитромицину в данном регионе свыше 15–20 %);
— схема ИПП + амоксициллин + метронидазол (может использоваться, если резистентность к метронидазолу в регионе меньше 40 %);
— 14-дневное назначение эрадикационной терапии увеличивает частоту эрадикации Нр на 9–12 % в сравнении с 7-дневным курсом;
— квадротерапию с коллоидным висмутом можно использовать как альтернативу терапии первой линии;
— в качестве схемы эрадикации второй линии сохранила свое значение квадротерапия на основе висмута как наиболее оптимальная.
В случае неэффективности схем эрадикации первой и второй линии ІІІ Маастрихтский консенсус предлагает практическому врачу несколько приемлемых вариантов дальнейшей терапии. Возможно назначение высоких доз амоксициллина (по 0,75 г 4 раза в сутки в течение 14 дней) в комбинации с высокими (4-кратными) дозами ИПП. Другим вариантом может быть замена метронидазола в схеме квадротерапии фуразолидоном (100–200 мг 2 раза в сутки). Альтернативной служит применение комбинации ИПП с амоксициллином и рифабутином (300 мг в сутки) или левофлоксацином (500 мг в сутки). Оптимальным путем преодоления резистентности Нр остается подбор антибиотиков с учетом индивидуальной чувствительности данного штамма Нр.
При НПВП-гастропатии, согласно ІІІ Маастрихтскому консенсусу, риск развития эрозий и язв желудка и двенадцатиперстной кишки у Нр-положительных больных выше, чем у Нр-отрицательных. Проведение эрадикационной терапии снижает риск развития язв и эрозий у больных, в связи с чем перед началом приема указанных препаратов необходимо проводить исследование инфицированности Нр и в случае ее подтверждения — назначать эрадикационную терапию. Однако проведения одной эрадикационной терапии недостаточно для предупреждения развития НПВП-гастропатий.
Антациды, особенно Маалокс, являются эффективными средствами борьбы с дуоденогастральным рефлюксом. Безусловно, при классической гастроэзофагеальной рефлюксной болезни антикислотная активность антацидов не может сравниться с таковой ИПП. Но при наличии билиарного рефлюкса целью их назначения является не только нейтрализация соляной кислоты, но и адсорбция желчных кислот и лизолецитина, а также повышение устойчивости слизистой оболочки к действию агрессивных факторов (цитопротекция). Этим требованиям отвечает, в частности, препарат Маалокс, в состав которого входят гидроокись алюминия и гидроокись магния в соотношении 1. 1 (таблетки) и 1,1. 1 (суспензия). Маалоксадсорбирует лизолецитин и желчные кислоты на 59–96 %. Он обладает продолжительным (до 4–6 часов) действием, адсорбирует не только соляную кислоту, образуя с ней буферные соединения, но и пепсин, желчные кислоты и лизолецитин. Известно, что в повреждающем действии на слизистую оболочку желудка и пищевода соляная кислота и компоненты желчи конкурируют за право считаться более агрессивным агентом.
Цитопротекторы. Известно, что слизистый протекторный барьер желудка имеет две линии защиты. Первая линия включает слизь, желудочную и дуоденальную секрецию бикарбонатов, гидрофобную поверхность слизистой оболочки желудка и двенадцатиперстной кишки. Вторую линию защиты образует эпителиальный барьер. Апикальная поверхность покровного желудочного эпителия и межклеточные соединения чрезвычайно устойчивы к обратной диффузии ионов Н+ благодаря наличию на их базолатеральных поверхностях двух транспортных систем, выводящих ионы Н+ из слизистой оболочки желудка. Целостность данного барьера регулируется желудочными факторами роста, одним из которых является трансформирующий фактор роста. В состав данного барьера входят тканевые субстанции, содержащие сульфгидрильные группы (глутатион- и тиолсодержащие протеины), являющиеся мощными естественными антиоксидантами, а также ловушками для свободных радикалов водорода и кислорода. Третья линия защиты включает нормальный кровоток, который способствует элиминации ионов Н+, обеспечивает энергией метаболические процессы, поддерживает первую и вторую линии защиты, а также регулирует репаративные процессы в слизистой оболочке желудка.
Для восстановления защитных свойств слизистой оболочки желудка используются цитопротекторы, например, вентер, сукральфат. Маалокс также обладает цитопротекторной активностью, что является важным в лечении эрозивных поражений гастродуоденальной зоны как за счет образования защитного слоя препарата на поверхности эпителия, так и в результате повышения выработки эндогенных простагландинов в слизистой оболочке желудка. Магния гидроксид повышает резистентность слизистой оболочки желудка и усиливает слизеобразование, а алюминия гидроксид создает защитную пленку и усиливает выработку простагландинов. Комбинация алюминия и магния в препарате Маалокс обеспечивает дополнение гаммы положительных свойств каждого антацидного компонента в отдельности и нивелирование отрицательных сторон алюминия и магния гидроокиси.
Значительный клинический эффект получен при лечении гастродуоденальных эрозий при назначении по 800 мг в сутки в течение 2–4 недель синтетических ПГ энпростила и мизопростола, которые улучшают региональный кровоток и микроциркуляцию, стимулируют образование слизисто-бикарбонатного барьера. Кроме простагландинов, цитопротекторным действием обладают также препараты висмута (в основном висмута трикалия дицитрат — де-нол), сукральфат, пентоксифиллин.
Препараты, улучшающие микроциркуляцию. Наибольшей эффективностью обладает трентал, улучшающий микроциркуляцию, реологические свойства крови и снабжение тканей кислородом. В единичных работах можно встретить рекомендации о включении в схемы лечения больных с хроническими эрозиями желудка иммунокорректоров — Т-активина по 100 мг в сутки в течение 5–10 дней, В-лейкина (человеческого рекомбинантного интерлейкина), галавита по 200 мг в сутки в течение 5–10 дней. Имеются сообщения об эффективности применения при хронических эрозиях желудка опиоидного пептида — даларгина и солкосерила, особенно в комплексе с антисекреторными препаратами.
Таким образом, хронические эрозии желудка отличаются рецидивирующим течением и, несмотря на большое количество медикаментозных средств и схем их применения, часто резистентны к проводимой терапии.
Нередко эффективность лечения больных с хроническими эрозиями остается низкой, в 24–25 % случаев не удается достичь клинико-эндоскопической ремиссии, что может привести к развитию серьезных осложнений. Все это свидетельствует о необходимости проведения более глубоких исследований этиологии и патогенеза хронических эрозий желудка с соблюдением принципа комплексности. Это позволит выбрать оптимальную схему лечения больных и существенно сократить сроки эпителизации хронических эрозий желудка. Дальнейшее динамическое наблюдение дает возможность снизить частоту рецидивирования хронических эрозий и улучшить качество жизни пациентов.
